



 智慧小复习系列答案
智慧小复习系列答案科目:初中化学 来源: 题型:阅读理解
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元?t-1) | 2305.00 | 1200.00 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
某化学课外活动小组欲从含少量泥沙、氯化镁、氯化钙等杂质的粗盐中得到精盐,设计了如下方案:
方案1:溶解→过滤→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
方案2:溶解→过滤→加入过量NaOH→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
方案3:溶解→过滤→加入过量石灰乳→加入过量Na2CO3→过滤→加入适量HCl,调节pH→蒸发
相关信息
信息一:石灰乳中含有较多未溶解的Ca(OH)2
信息二:部分物质溶解性:MgCO3微溶、CaCO3难溶、Mg(OH)2难溶、Ca(OH)2微溶
信息三:部分化学试剂的市场价格
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元?t-1) | 2305.00 | 1200.00 |
请根据题目要求及以上信息,回答下列问题:
(1)上述每个方案都设计了两次过滤,第一次过滤的作用是______;每个方案中都设计要调节pH,其值为______.
(2)通过分析,活动小组的同学认为上述方案3设计是最合理的.那么方案3优于方案2的理由是______,
方案l的不足之处是______.
方案3中发生反应的化学方程式为______;______.(写出其中两个)
(3)方案3中选用石灰乳而不选用澄清石灰水的原因是______.
A.澄清石灰水中含Ca(OH)2较少,石灰乳中含Ca(OH)2较多
B.澄清石灰水中Ca(OH)2的浓度较小,选用澄清石灰水稀释了原溶液,使蒸发时间延长
C.石灰乳中溶解了的Ca(OH)2不断参与反应,未溶解的Ca(OH)2不会溶解补充
D.石灰乳中溶解了的Ca(OH)2不断参与反应,未溶解的Ca(OH)2不断溶解补充.
查看答案和解析>>
科目:初中化学 来源:仙桃 题型:问答题
| 试剂 | NaOH | Ca(OH)2 |
| 价格(元?t-1) | 2305.00 | 1200.00 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
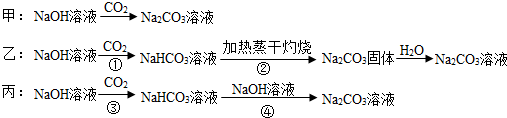
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com