
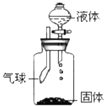
 用如图的装置进行实验,使固体与液体接触,能够观察到气球先膨胀,过一段时间又恢复到原状,符合条件的一组物质是( )
用如图的装置进行实验,使固体与液体接触,能够观察到气球先膨胀,过一段时间又恢复到原状,符合条件的一组物质是( )| A. | 硝酸铵和水 | B. | 生石灰和水 | ||
| C. | 碳酸钠和稀盐酸 | D. | 二氧化锰和过氧化氢溶液 |
分析 根据物质的性质以及压强知识进行分析,密闭容器内小气球鼓起,则是物质间结合产生气体或放出热量,使装置内的压强变大,过一段时间又恢复到原状,说明装置内的压强恢复与原来相等.
解答 解:
A、硝酸铵固体溶于水吸收热量,使装置内的压强变小,不会出现气球变大的现象,故A错误;
B、生石灰与水反应放出大量的热,使装置内的压强变大,小气球鼓起,过一段时间热量散失,气温恢复到原来的温度,则压强恢复与原来相等,气球恢复原状,故B正确;
C、固体碳酸钠能与盐酸反应生成二氧化碳气体,使装置内的压强增大,气球鼓起,但是生成的二氧化碳不会消失,因此不会出现气球恢复原状的现象,故C错误;
D、二氧化锰和过氧化氢溶液反应生成氧气,装置内的压强增大,气球鼓起,但是生成的氧气不会消失,因此不会出现气球恢复原状的现象,故D错误;
答案:B
点评 本题考查了常见物质的性质,完成此题,可以依据已有的知识进行,要能将学科间的知识结合起来进行正确的解题.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:选择题
| A. | NaCl、KNO3、(NH4)2SO4 | B. | HCl、AgNO3、Na2SO4 | ||
| C. | CuCl2、Fe2(SO4)3、NaNO3 | D. | NaCl、K2CO3、NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用酒精温度计测得某溶液温度为25.68°C | |
| B. | 用10mL量筒量取98%稀H2SO4溶液3.68mL | |
| C. | 用“pH计”测得某血浆的pH=7.40 | |
| D. | 用托盘天平称取5.85g粗盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Zn | B. | CuO | C. | CO2 | D. | Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
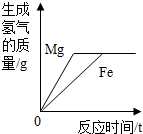 取等质量的镁和铁两种金属.将镁放入稀硫酸中,铁放入稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.下列说法正确的是( )
取等质量的镁和铁两种金属.将镁放入稀硫酸中,铁放入稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.下列说法正确的是( )| A. | 消耗铁的质量一定小于镁的质量 | |
| B. | 充分反应后,镁、铁一定都有剩余 | |
| C. | 充分反应后,稀硫酸和稀盐酸一定都没有剩余 | |
| D. | 充分反应后,溶液的质量一定都有所增加 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
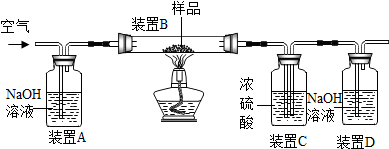
| 装置B | 装置C | 装置D | |
| 实验前物质的质量/g | 180.0 | 200.0 | 122.2 |
| 实验后物质的质量/g | 176.9 | 201.5 | 124.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com