
【题目】现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成.为确定其组成,进行了如图所示的实验(假设实验过程无损耗). 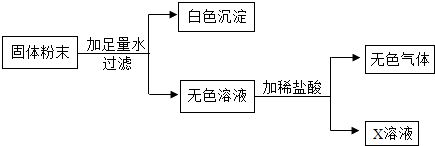
请回答:
(1)根据实验可以确定白色沉淀是;原固体粉末中一定含有 , 它的可能组成有种.
(2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是g,固体粉末由(填化学式,下同)组成,其中质量小于10g的是 .
【答案】
(1)CaCO3;Na2CO3;3
(2)11.7;CaCO3、CaO、Na2CO3;CaCO3、CaO
【解析】解:(1)在白色粉末中能产生白色沉淀,可知该白色沉淀应该为碳酸钙,又得到的无色溶液能够和稀盐酸反应生成气体,可以知道在固体粉末中一定含有碳酸钠,所以可以判断,碳酸钙可能是原混合物中含有的,也可能是氧化钙与水反应后生成的氢氧化钙和碳酸钠反应生成的,所以它的可能的组合为:①碳酸钙、碳酸钠、氧化钙; ②碳酸钠,碳酸钙;③碳酸钠、氧化钙等三种可能的组成;(2)根据(1)的解答可知X溶液为氯化钠溶液其质量为:200g×5.85%=11.7g,根据题意结合化学方程式,可以求出与盐酸反应的碳酸钠的质量为10.6g,进而可以判断出该固体粉末的组成为:CaCO3、CaO、Na2CO3 , 进而可以判断若白色沉淀质量小于10g,则原混合物的组成为氧化钙和碳酸钙,计算过程如下: 解:设碳酸钠的质量为x,则:
Na2CO3+2HCl═ | 2NaCl+H2O+CO2↑ |
106 | 117 |
x | 11.7g |
![]()
解得x=10.6g
这里我们求得的只是和盐酸反应的碳酸钠,总质量为20g,所以假如白色沉淀是固体粉末中的,则只有20g﹣10.6g=9.4g,而题目中得到的白色沉淀的质量是10g,也就是说白色沉淀并不是完全来自于原固体粉末中,而是有一部分是反应中生成的,即氧化钙和水反应生成了氢氧化钙,而氢氧化钙又和碳酸钠反应生成了碳酸钙沉淀,从而可以判断在混合物中含有氧化钙.
故本题答案为:(1)CaCO3; Na2CO3;3;(2)11.7; CaCO3、CaO、Na2CO3;CaCO3、CaO.


科目:初中化学 来源: 题型:
【题目】汽车是现代生活中不可缺少的代步工具.请回答下列问题:
(1)汽车电路中的导线多数是用铜制做的,这是利用了金属铜的导电性和性.
(2)下列汽车配件及用品中,用合金制做的是(填字母) . 
(3)铁在潮湿的空气中容易锈蚀. ①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝空气(氧气)和 .
②喷漆前需将铁制品放人稀盐酸中除锈(铁锈主要成分是Fe2O3),反应初期可观察到溶液由无色变为黄色,这是因为生成了(填化学式)的缘故;反应进行一会儿,又可以观察到有无色气泡产生,该反应的化学方程式是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质之间的转化能够实现的是( )
A.CuO ![]() Cu
Cu ![]() CuO
CuO
B.CaCO3 ![]() CaCl2
CaCl2 ![]() Ca(NO3)2
Ca(NO3)2
C.Fe ![]() Fe2O3
Fe2O3 ![]() FeCl3
FeCl3
D.Al2O3 ![]() Al(OH)3
Al(OH)3 ![]() AlCl3
AlCl3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸可发生反应:4HNO3 ![]() 4NO2↑+X+2H2O.据此回答:
4NO2↑+X+2H2O.据此回答:
(1)反应的基本类型属于反应;
(2)X的化学式为 , 推断的依据为;
(3)硝酸的保存应注意、 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你参与下列探究: 【问题情景】在课外活动中,小斌按照课本实验(见图1)探究分子的运动时,闻到了刺激性的氨味,于是,小斌在老师的指导下,设计了如图2的实验装置,进行同样的实验,结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论.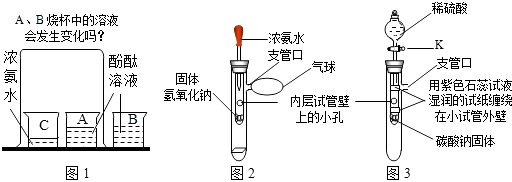
【实验探究与结论】小斌用图2装置进行实验.
(1)滴入少量浓氨水后,湿润的酚酞滤纸条发生的变化是 . 从分子运动的角度分析,此现象可说明的结论是;从浓氨水化学性质的角度分析,此现象可说明的结论是 .
(2)用初中的化学知识分析,固体氢氧化钠的作用是 .
(3)和课本实验比较,小斌改进后的装置的优点是(写出两点)①;② .
(4)【思维拓展】小媚受小斌实验的启发,将图2装置进一步改装成图3装置,用于验证二氧化碳的性质. 打开活塞K滴入稀硫酸后,两条用紫色石蕊试液润湿的试纸发生的相同变化是 , 不同变化是 , 小媚从课本实验中知道,二氧化碳和水本身都不能使石蕊变色,因而她认为以上两个变化验证的二氧化碳的性质依序是、 .
(5)小柔认为小媚的装置还可以同时验证:①二氧化碳能使澄清石灰水变浑浊;②二氧化碳不能燃烧,也不支持燃烧. 小柔为完成自己的两个验证实验,对小媚的实验进行的简单改进是:、
.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映所对应叙述关系的是( ) 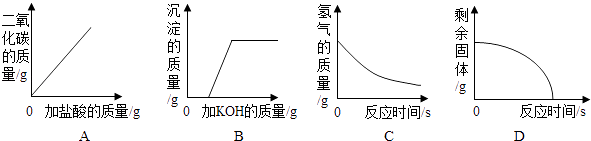
A.向一定量大理石中滴加稀盐酸
B.向HCl和CuCl2混合液中滴加KOH溶液
C.一定量的稀硫酸与锌粒反应
D.煅烧一定质量的石灰石
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课外小组同学,用如图所示实验验证质量守恒定律. 
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上.最后天平的指针(填序号)(a.偏左 b.偏右 c.不偏转 d.无法预测).
(2)乙同学用B装置研究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上.发现天平的指针偏右.
①造成天平的指针向右偏转的原因是 .
②若将本实验中的烧杯替换成带有气球的锥形瓶,如图C所示,其他操作不变,最后天平平衡.可见,在验证质量守恒定律时,若利用有气体参加或有气体生成的要考虑气体质量.
(3)在化学反应前后,一定不变的是(填序号).
①元素种类 ②原子种类 ③原子数目 ④分子种类 ⑤分子数目 ⑥物质的总质量
(4)应用质量守恒定律可以确定反应物或产物的化学式.在载人宇宙飞船中,一般都安装盛放过氧化钠(Na2O2)颗粒的装置,它的作用是再生氧气,供宇航员呼吸,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+X.则X的化学式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com