
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入氢氧化钠溶液质量(克) | 40 | 40 | 40 | 30 |
| 生成沉淀的总质量(克) | 0 | 4.9 | 9.8 | 9.8 |
分析 (1)根据溶液稀释前后,溶质质量不变进行分析;
(2)根据硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠进行分析;
(3)根据生成沉淀氢氧化铜沉淀的质量和化学方程式进行计算;
(4)根据先加入的氢氧化钠会与硫酸反应生成硫酸钠和水,以及调整的数据进行计算;
(5)根据反应后所得溶液的溶质质量和溶液质量进行计算;
(6)根据废液中铜元素的质量分数进行计算.
解答 解:(1)要用30%的氢氧化钠溶液来配置实验中所需的150g氢氧化钠溶液,需要加水的质量为
150g-$\frac{150g×10%}{30%}$=100g;
(2)硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)通过表中的数据可知,生成沉淀的最大量是9.8g
设参加反应的硫酸铜质量为x,消耗氢氧化钠质量为y,生成硫酸钠质量为m,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160 80 98 142
x y×10% 9.8g m
$\frac{160}{x}$=$\frac{98}{9.8g}$=$\frac{80}{y×10%}$=$\frac{142}{m}$
x=16g
y=80g
m=14.2g
(4)通过分析可知,与硫酸铜反应的氢氧化钠质量为80g,加入40g的氢氧化钠没有出现沉淀,所以与硫酸反应的氢氧化钠质量为z,生成硫酸钠质量为n
H2SO4+2NaOH=Na2SO4+2H2O
98 80 142
z 40g×10% n
$\frac{98}{z}$=$\frac{80}{40g×10%}$=$\frac{142}{n}$
z=4.9g
n=7.1g
所以该混合溶液中硫酸的质量分数为:$\frac{4.9g}{100g}$×100%=4.9%;
(5)所以反应溶液质量分数为:$\frac{14.2g+7.1g}{100g+120g-9.8g+2.8g}$×100%=10%;
(6)从200吨废液中提取金属铜,则理论上可以提取金属铜的质量为:200t×$\frac{\frac{64}{98}×9.8g}{100g}$=12.8t.
故答案为:(1)100g;
(2)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)$\frac{160}{x}$=$\frac{98}{9.8g}$;
(4)4.9%;
(5)10%;
(6)12.8t.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | 氯化钡溶液、盐酸 | B. | 酚酞、铁片 | ||
| C. | 酚酞、盐酸 | D. | 石蕊试液、氯化钙溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
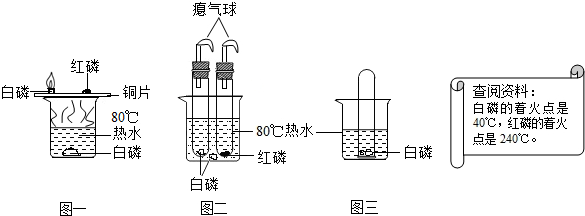
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用观察颜色区分硫酸铜溶液和硫酸亚铁溶液 | |
| B. | 用水区分硝酸铵固体和氢氧化钠固体 | |
| C. | 用闻气味区别氧气和空气 | |
| D. | 用稀硫酸区分黄铜(Cu、Zn)和黄金 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
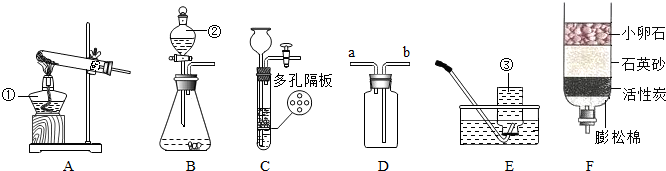 (1)写出带标号仪器的名称:①酒精灯,②分液漏斗,③集气瓶.
(1)写出带标号仪器的名称:①酒精灯,②分液漏斗,③集气瓶.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
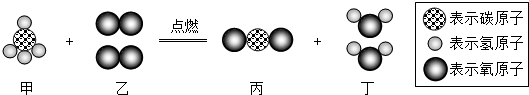
| A. | 该反应中分子和原子的种类都发生了改变 | |
| B. | 物质甲的化学式是CH4 | |
| C. | 甲、乙两物质参加反应的质量比为1:2 | |
| D. | 图示反应属于化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com