
【题目】某同学用如图所示的装置探究质量守恒定律,锥形瓶内是红磷。

(1)反应前锥形瓶内红磷和氧气的质量总和不一定等于反应后生成五氧化二磷的质量,为什么______________?
(2)实验过程中气球鼓起,实验后比实验前还瘪。请解释气球发生上述变化的原因______________。
【答案】如果红磷和氧气恰好完全反应,生成的五氧化二磷的质量等于红磷和氧气的质量总和。如果红磷剩余或氧气剩余,生成的五氧化二磷的质量小于红磷和氧气的质量总和 红磷燃烧放出热量,导致锥形瓶中压强增大,气球膨胀。反应后冷却至室温时,由于氧气被消耗,锥形瓶中压强减小,小于外界压强,气球缩小,并且实验后比实验前还瘪
【解析】
(1)反应前锥形瓶内红磷和氧气的质量总和不一定等于反应后生成五氧化二磷的质量,是因为红磷和氧气不恰好完全反应时红磷和氧气的质量总和大于反应后生成五氧化二磷的质量;
(2)实验过程中气球鼓起,实验后比实验前还瘪,原因:红磷燃烧放热,气压增大,导致气球膨胀;完全反应后氧气消耗,温度降低,锥形瓶中压强减小,小于外界压强,气球缩小,并且实验后比实验前还瘪。


 小题狂做系列答案
小题狂做系列答案科目:初中化学 来源: 题型:
【题目】小陈在探究氯化钙的性质,进行图甲所示的实验。 试验后,他向反应后的溶液中逐滴滴加碳酸钠溶液,溶液pH的变化如图所示,下列分析正确的是( )
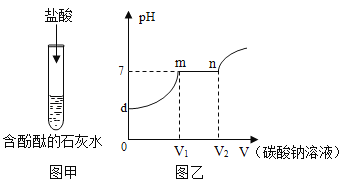
A. 图甲中实验仪器操作无误
B. 图乙中d﹣m段反应过程中有沉淀产生
C. 图乙中m﹣n段反应过程中有气泡产生
D. 图乙中n 点之后溶液中的溶质有 Na2CO3 和 NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室可以用高锰酸钾制取氧气并探究氧气的性质。
(1)如何验证一瓶无色气体是氧气___________?
(2)铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是什么___________?
(3)实验室用高锰酸钾制取氧气,有如下操作步骤:
①加热;②检查装置的气密性;③装药品;④用排水法收集氧气;⑤从水槽中取出导管;⑥熄灭酒精灯:正确的排序为:___________
(4)写出高锰酸钾制取氧气的文字或者符号表达式___________,并在下图将发生装置补充完整___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。
⑴贝贝取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。结论:石蜡的密度比水 ;
⑵芳芳点燃蜡烛,观察到火焰分为外焰、内焰、焰心三层。把一根火柴梗放在火焰中(如图)约1s后取出可以看到火柴梗的 (填“a”、“b”或“c”)处最先碳化。结论:蜡烛火焰的 温度最高;
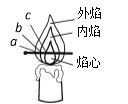
⑶婷婷在探究蜡烛燃烧的过程中,发现罩在火焰上方的烧杯内壁被熏黑,你认为她的以下做法中不合适的是( )
A.反复实验,并观察是否有相同现象
B.查找资料,了解石蜡的主要成分,探究生成的黑色固体是什么
C.认为与本次实验目的无关,不予理睬
D.询问老师或同学,讨论生成黑色物质的原因
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是
A. 叶酸的相对分子质量为441 g
B. 叶酸中氮元素的质量分数大于氧元素的质量分数
C. 叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D. 叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小兵带回一瓶浑浊山泉水,他在实验室模拟自来水厂净水过程,最终制成蒸馏水,流程如图:
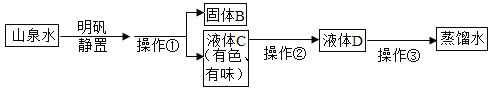
(1)操作①的名称是_________(填操作名称),实验室进行该操作时玻璃棒的作用是_________,该操作需要的玻璃仪器除玻璃棒外,还需要_________;(填仪器名称)若经过操作①后,所得液体C中仍有浑浊,其原因可能是_________(填序号);
a漏斗内的滤纸有破损 b漏斗下端未靠在烧杯内壁 c漏斗内液面高于滤纸的边缘
(2)操作②主要是除去一些异味和色素,应选用的物质是__________________(填名称);
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较少泡沫,说明液体D是_________,(填“硬水”或“软水”),操作③其净水效果最佳,是_________(填操作名称)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:

(1)P点的含义是______________________________。
(2)t2℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?______________________(填写“能”或“不能”)。
(3) t2℃时等质量的a、b、c三种物质的饱和溶液中溶剂质量由小到大的顺序排列是_____________________(填写物质序号)。
(4)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是______(填写选项序号)。
A c>a=b B a=b>c C a>b>c D b>a>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习质量守恒定律的内容时, 我们曾经做了如图所示的实验, 回答下列问题(已知:Na 2 CO 3 +2HCl=2NaCl+CO 2↑ +H 2O):
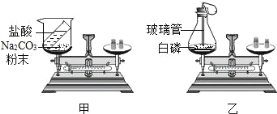
(1)图甲中反应后天平的指针_____(“偏左”“偏右”“不变”),原因是_____,该反应是否符合质量守恒定律?_____(填“符合”或“不符合”)。
(2)图乙中在实验设计时,锥形瓶底放层细沙的原因是:防止锥形瓶______;化学方程式为_____;白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡。结论是:质量不守恒。待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡。结论是:质量守恒。你认为结论正确的是______填“前一种”或“后一种”)
(3)由以上实验可知,用有气体参加或生成的反应来验证质量守恒定律时,反应必须在_________中进行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小宇查阅资料得知:氯酸钾在二氧化锰、氧化铁等物质作催化剂条件下可生成氯化钾和氧气。于是,他对影响氯酸钾分解的因素及催化剂的效果产生了探究兴趣。
(提出问题)氧化铁是否比二氧化锰催化效果更好?
(设计实验)小宇以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3 | 其它物质的质量 | 温度 | 收集氧气的体积 | 反应时间 |
① | 10.0g | 无 | 330℃ | 100mL | t1 |
② | 10.0g | 氧化铁1.5g | 330℃ | 100mL | t2 |
③ | 10.0g | 二氧化锰1.5g | 330℃ | 100mL | t3 |
④ | 10.0g | 二氧化锰xg | 380℃ | 100mL | t4 |
(结论与反思)
(1)若t1________t2(选填“>”、“=”或“<”),说明氧化铁能加快氯酸钾的分解速率。若要确定氧化铁是氯酸钾分解反应的催化剂,还需探究反应前后氧化铁的________和________不变。
(2)若t2>t3,说明氧化铁对氯酸钾分解的催化效果比二氧化锰________(填“强”或“弱”)。
(3)写出实验④所涉及反应的化学方程式__________________。
(4)实验④中MnO2的质量x为________g,若t3 > t4,则化学反应速率与温度的关系是______________。
(5)氯酸钾的分解速率可能还与_____________________因素有关,需设计实验进一步证明。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com