
| A. | 滴加CaCl2溶液 | B. | 滴加稀盐酸 | C. | 滴加Ca(OH)2溶液 | D. | 滴加石蕊试液 |
分析 题目要求证明NaOH中含有Na2CO3,这就需要利用Na2CO3自己的独有的性质,而不能借助和NaOH相同性质,更不能利用NaOH自己独有的性质,所以要从给定的实验中进行选择.
解答 解:A、滴加CaCl2溶液时,由于CaCl2溶液能够与和Na2CO3反应生成白色沉淀,能证明溶液中含有Na2CO3,故A正确.
B、滴加稀盐酸,与氢氧化钠反应无现象,而与Na2CO3则生成气体,HCl+NaOH=NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑,能够证明.故正确.
C、滴加Ca(OH)2溶液,Ca(OH)2溶液能够与和Na2CO3反应生成白色沉淀,能证明溶液中含有Na2CO3,故C正确.
D、滴加石蕊试液,由于NaOH和Na2CO3的溶液都显碱性,所以都能够使石蕊变红蓝色,无法证明.故D错误.
故选D.
点评 物质区别或者检验时要注意选择检验物质所独有的性质,这就要求在选择试剂时对物质的性质进行对比后借助性质差异来进行.


科目:初中化学 来源: 题型:选择题
| A. | ②④ | B. | ①② | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在氢气中,氢元素的化合价为+1价 | |
| B. | 在氯化钠中,钠元素的化合价为-1价 | |
| C. | 在二氧化硅中,氧元素的化合价为+2价 | |
| D. | 化合价是元素的原子在形成化合物时表现出的一种性质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在氧气中燃烧时,发出微弱的淡蓝色火焰 | |
| B. | 铁丝在氧气中燃烧时,火星四射,生成红色固体 | |
| C. | 镁条在空气中燃烧时,发出耀眼的白光,生成白色固体 | |
| D. | 红磷在空气中燃烧时,产生大量白色烟雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
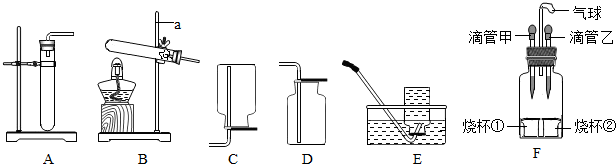
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
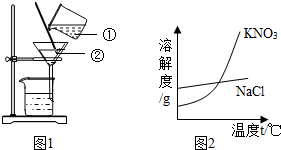 图1为精制粗盐的示意图,回答:
图1为精制粗盐的示意图,回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
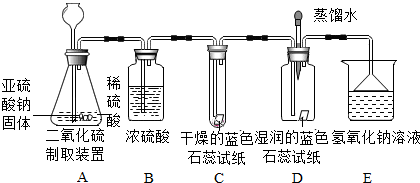
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com