
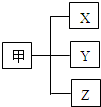
 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( ) | 选项 | 甲 | X | Y | Z |
| A | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
| B | 常见的矿物燃料 | 煤 | 石油 | 天然气 |
| C | 常见的合金 | 钢铁 | 生铁 | 氧化铁 |
| D | 常见的行星 | 地球 | 太阳 | 月球 |
| A. | A | B. | B | C. | C | D. | D |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 加热 | B. | 加入适量纯碱 | C. | 加入适量氯化钡 | D. | 加入适量明矾 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加大城市绿化园林建设 | B. | 禁止焚烧桔杆 | ||
| C. | 大力发展火力发电 | D. | 建筑工地,定时洒水降尘 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
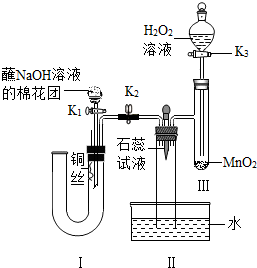 某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)
某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
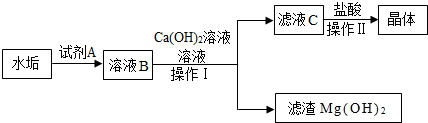
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
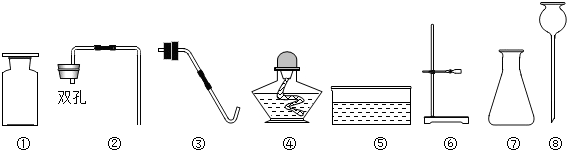
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com