


科目:初中化学 来源: 题型:
| A、用石灰浆涂抹墙壁后,墙壁表面出现大量水珠 |
| B、在口中咀嚼米饭或馒头时感到有甜味 |
| C、用干冰做制冷剂进行人工降雨 |
| D、鸡蛋壳在食醋中浸泡后逐渐变软 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、木糖醇中含有5个碳原子、12个氢原子和5个氧原子 |
| B、木糖醇中碳、氢、氧元素的质量比为5:12:5 |
| C、木糖醇中氢元素的质量分数最大 |
| D、木糖醇由碳、氢、氧三种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室常用高锰酸钾粉末制取氧气(装置A),也可用过氧化氢溶液和催化剂二氧化锰粉末来制取氧气(装置B).装置B中的仪器a是分液漏斗,通过活塞的“开”、“关”可以随时滴加过氧化氢溶液,从而控制得到氧气的质量.
实验室常用高锰酸钾粉末制取氧气(装置A),也可用过氧化氢溶液和催化剂二氧化锰粉末来制取氧气(装置B).装置B中的仪器a是分液漏斗,通过活塞的“开”、“关”可以随时滴加过氧化氢溶液,从而控制得到氧气的质量.| 装置A | 装置B | |
| 所需药品状态 | ||
| 反应条件 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 验证方法及操作 | 可能看到的现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
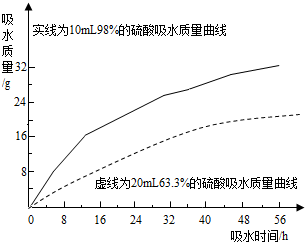 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:| 方案 | 实验假设 | 实验方案 | 实验现象与结论 |
| Ⅰ | 能发 生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中. | 无明显变化,假设成立. |
| Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中. | 假设成立. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com