
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 充分反应后生成气体的质量/g | 1.1 | 2.2 | X | 3.08 | 3.08 |
分析 (1)分析图表烧杯①②数据可知,每加入10g稀盐酸生成气体的质量为1.1g,则加入30g稀盐酸生成气体的质量为3.3g,由烧杯④⑤加入的盐酸大于30g时只产生了3.08g气体,说明了x的值应是3.08g;
(2)利用碳酸钙与盐酸反应的化学方程式和生成气体的质量,列出比例式,就可计算出样品中碳酸钙的质量,然后根据质量分数公式计算即可.
(3)根据质量守恒定律烧杯④中物质充分反应后所得溶液的质量.
解答 解:(1)分析图表烧杯①②数据可知,每加入10g稀盐酸生成气体的质量为1.1g,则加入30g稀盐酸完全反应生成气体的质量为3.3g,由烧杯④⑤加入的盐酸大于30g时只产生了3.08g气体,说明了x的值应是3.08g;
(2)设10g样品中碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.08g
∴$\frac{100}{44}=\frac{x}{3.08g}$ 解之得:x=7g.
则此“石头纸”中碳酸钙的质量分数为:$\frac{7g}{10g}$×100%=70%.
(3)烧杯④中物质充分反应后所得溶液的质量为:7g+40g-3.08g=43.92g
答:(1)3.08;(2)样品中碳酸钙的质量分数为70%;(3)43.92.
点评 本题主要考查学生从图表获得有效数据结合化学方程式进行计算的能力.要求学生有较强的识图能力和数据分析能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
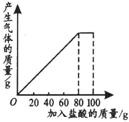 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图象.| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来.一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.单质碳也具有还原性,碳还原氧化铁的化学方程式为3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2,如图装置的反应中,实验开始前应先通CO(选填“通CO”或“加热”).
铁矿石冶炼成铁是一个复杂的过程,把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来.一氧化碳还原氧化铁的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.单质碳也具有还原性,碳还原氧化铁的化学方程式为3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2,如图装置的反应中,实验开始前应先通CO(选填“通CO”或“加热”).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 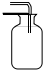 导管伸入到集气瓶体积的$\frac{1}{3}$处 | B. |  导管伸入到集气瓶体积的$\frac{2}{3}$处 | ||
| C. |  集气瓶中灌$\frac{2}{3}$的水 | D. | 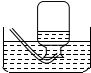 集气瓶中灌$\frac{1}{3}$的水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com