
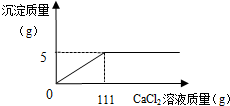
 某碳酸钠和氯化钠的混合粉末21.2g,不断加入CaCl2溶液,产生沉淀的质量与所加入的CaCl2溶液的关系如图所示.
某碳酸钠和氯化钠的混合粉末21.2g,不断加入CaCl2溶液,产生沉淀的质量与所加入的CaCl2溶液的关系如图所示.分析 根据所加入的CaCl2溶液与碳酸钠发生反应生成碳酸钙沉淀和氯化钠;由变化曲线图可知,生成的沉淀质量为5g;根据反应的化学方程式,可以计算碳酸钠的物质的量和质量分数.
解答 解:①由变化曲线图可知,生成的碳酸钙沉淀质量为5g,则设混合粉末中碳酸钠的质量为x.
CaCl2+Na2CO3=2NaCl+CaCO3↓
106 100
x 5g
则$\frac{106}{100}=\frac{x}{5g}$,解得x=5.3g.
故混合粉末中碳酸钠的物质的量为$\frac{5.3g}{106g/moL}$=0.05moL,
②原粉末中碳酸钠的质量分数为$\frac{5.3g}{21.2g}$×100%=25%.
故答案为:①0.05moL;②25%.
点评 变化曲线的起点是前一个反应恰好完全反应的终点也是后一个反应的起点,曲线折点则是与此曲线相关反应的终点.


科目:初中化学 来源: 题型:解答题
 孔明灯由叫天灯,它是一盏会漂浮的纸灯笼,现在人们燃放孔明灯(如图所示)多作为祈福之用.
孔明灯由叫天灯,它是一盏会漂浮的纸灯笼,现在人们燃放孔明灯(如图所示)多作为祈福之用.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
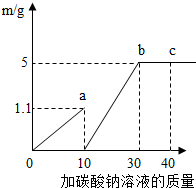 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 滴加NaOH溶液的质量/g | 9.0 | 9.4 | 9.8 | 10.0 | 10.2 |
| 溶液的pH | 1.8 | 2.1 | 2.6 | 7.0 | 11.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.0 | 35.0 | 35.0 | 35.0 |
| 剩余固体的质量/g | 6.821 | 5.6 | 4.4 | 4.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com