

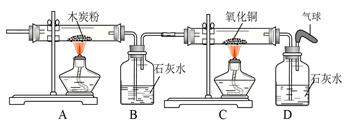
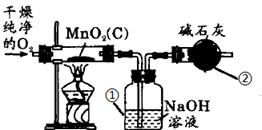
|
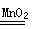 2H2O + O2↑ a 可以随时控制反应的发生和停止
2H2O + O2↑ a 可以随时控制反应的发生和停止  +H2O;
+H2O; CO2
CO2

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
 小刚根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;
小刚根据“蛋壳残渣质量为4.3g”,求得蛋壳中碳酸钙的质量分数为 ;查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
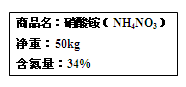
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的质量 | 18.25g | 36.5g | 47.9g |
| 生成气体的质量 | 2.2g | 4.4g | 4.4g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com