
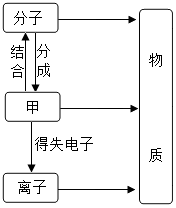
 初中化学学习中,我们初步认识了物质的微观结构.构成物质的粒子之间的关系如图所示:
初中化学学习中,我们初步认识了物质的微观结构.构成物质的粒子之间的关系如图所示: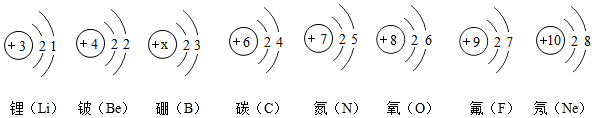
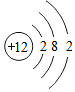 ,上图中与其化学性质相似的元素是Be.
,上图中与其化学性质相似的元素是Be.分析 根据物质的微观构成粒子、符号的书写以及化学符号周围数字的意义进行分析解答,在原子中,核內质子数等于核外电子数,元素的化学性质与原子的最外层电子数有关,据此解答.
解答 解:(1)甲是能构成分子,能形成离子,故甲是原子,故填:原子.
(2)在水,水银,硫酸铜三种物质中,氯化钠是由离子构成的物质,它由钠离子和氯离子组成,故填:氯化钠;钠离子和氯离子.
(3)2个钙离子就是在钙离子的前面加上数字2,故填:2Ca2+;
70个碳原子构成的一种新分子,就是在碳元素符号的右下角加上数字70,故填:C70;
保持氢气化学性质的最小粒子是氢分子,故填:H2;
水分子的符号为:H2O,故填:H2O;
(4)CO32-中“2”表示一个碳酸根离子带有2个单位的负电荷,故填:一个碳酸根离子带有2个单位的负电荷.
(5)①图中这些元素的原子核外有2个电子层,故都处于第2周期.在原子中核內质子数-核外电子数,故硼原子结构示意图中的X=2+3=5,故填:2;5.
②元素的化学性质与原子的最外层电子数有关,镁原子的结构示意图中最外层有2个电子,故图中与其化学性质相似的元素是Be,故填:Be.
这两种原子在化学反应中容易失去电子,故填:失去.
③图中元素从左到右排列所遵循的一条规律是核电荷数依次递增,故填:核电荷数依次递增.
④1个一氧化碳分子中所含电子总数为:6+8=14,故填:14.
点评 本题考查的是物质的微观构成粒子的知识,完成此题,可以依据已有的知识结合题干提供的信息进行.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
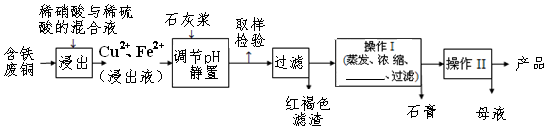
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com