解:(1)地壳中含量最多的金属元素是铝元素,氧化物是指含有两种元素其中一种是氧元素的纯净物,所以下列矿石的主要成分属于氧化物的是Fe
2O
3和Al
2O
3;
(2)①一氧化碳还原氧化铁生成铁和二氧化碳,化学方程式为Fe
2O
3+3CO

2Fe+3CO
2;
②向含有AgNO
3、Cu(NO
3)
2、Zn(NO
3)
2的混合溶液中加入一定量的铁粉,铁粉先和硝酸银溶液反应生成银和硝酸亚铁,反应完后再和硝酸铜溶液反应生成铜和硝酸亚铁,铁粉不和硝酸锌溶液反应,所以使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,说明一定金属铁有剩余,故滤液中一定含Fe
2+、Zn
2+,不含Cu
2+、Ag
+;
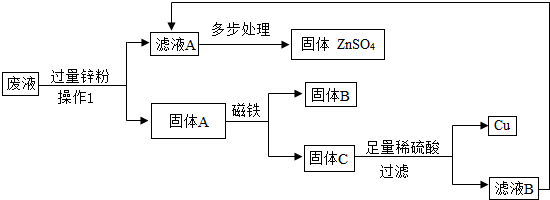
(3)锌先和硫酸铜溶液反应生成铜和硫酸锌,反应完后再和硫酸亚铁溶液反应生成铁和硫酸锌.
①过滤用于分离不溶性固体,所以操作1的名称是过滤;加入过量的锌粉,所以固体A的成分为 Zn、Fe、Cu;
②若要检验向固体C中加入的稀硫酸是否足量的方法是取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量;
③若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和操作1中加入锌粉的质量.
故答案为:(1)Al;Fe
2O
3、Al
2O
3;
(2)Fe
2O
3+3CO

2Fe+3CO
2;C;
(3)①过滤;Zn、Fe、Cu;
②取少量铜,加适量稀硫酸,若无气泡产生,证明硫酸足量;
③操作1中加入锌粉的质量.
分析:(1)根据地壳中含量最多的金属元素是铝元素以及氧化物是指含有两种元素其中一种是氧元素的纯净物进行解答;
(2)根据一氧化碳还原氧化铁生成铁和二氧化碳以及向含有AgNO
3、Cu(NO
3)
2、Zn(NO
3)
2的混合溶液中加入一定量的铁粉,铁粉先和硝酸银溶液反应生成银和硝酸亚铁,反应完后再和硝酸铜溶液反应生成铜和硝酸亚铁,铁粉不和硝酸锌溶液反应进行解答;
(3)根据锌先和硫酸铜溶液反应生成铜和硫酸锌,反应完后再和硫酸亚铁溶液反应生成铁和硫酸锌进行解答.
点评:仔细审题,有题意可知一些信息,根据信息推导做题;利用金属活动性顺序,回收工业重要原料硫酸锌和有关金属.

 2Fe+3CO2;
2Fe+3CO2; 2Fe+3CO2;C;
2Fe+3CO2;C;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案