
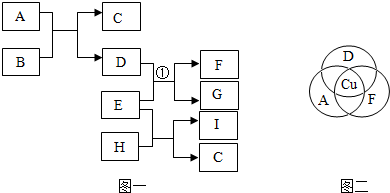
分析 根据A~I表示初中化学常见的物质,Ⅰ俗称纯碱,所以I是碳酸钠,A、D、F三种物质中都含有铜元素,E和H会生成碳酸钠和C,所以E可以是氢氧化钠,H是二氧化碳,C就是水,A和B反应会生成水和E,所以A可以是氧化铜,B是盐酸,盐酸和氧化铜反应生成氯化铜和水,所以D是氯化铜,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,所以F是氢氧化铜,G是氯化钠,然后将推出的物质进行验证即可.
解答 解:(1)A~I表示初中化学常见的物质,Ⅰ俗称纯碱,所以I是碳酸钠,A、D、F三种物质中都含有铜元素,E和H会生成碳酸钠和C,所以E可以是氢氧化钠,H是二氧化碳,C就是水,A和B反应会生成水和E,所以A可以是氧化铜,B是盐酸,盐酸和氧化铜反应生成氯化铜和水,所以D是氯化铜,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,所以F是氢氧化铜,G是氯化钠,经过验证,推导正确,所以I是Na2CO3;
(2)通过推导可知,E是氢氧化钠,在化学实验中常用作干燥剂;
(3)通过推导可知,A~I中属于氧化物的有水、氧化铜、二氧化碳3种;
(4)反应①是氢氧化钠和氯化铜反应生成氢氧化铜沉淀和氯化钠,化学方程式为:2NaOH+CuCl2=Cu(OH)2↓+2NaCl.
故答案为:(1)Na2CO3;
(2)干燥剂;
(3)3;
(4)2NaOH+CuCl2=Cu(OH)2↓+2NaCl.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:选择题
| A. |  树根“变”根雕 | B. |  葡萄“变”美酒 | ||
| C. |  玉石“变”印章 | D. |  玩具机器人“变”形 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| A中浓硫酸浓度 | 实验现象 | A中生成 气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验Ⅰ | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验Ⅱ | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验Ⅲ | 20% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
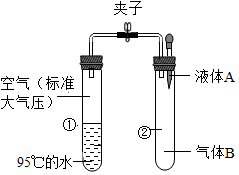 如图所示,夹子开始处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了,则液体A与气体B的组合不可能是( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了,则液体A与气体B的组合不可能是( )| A. | 酒精、氧气 | B. | 水、氨气 | ||
| C. | 硝酸银溶液、氯化氢 | D. | 氢氧化钠溶液、二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
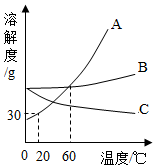 如图为A、B、C三种固体物质的溶解度曲线,回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com