
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;该反应放出大量的热,属于放热反应.
(2)铁和硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(3)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;在发生装置的试管口放一团棉花的作用是防止加热时高锰酸钾粉末进入导管.
(4)氨水与硫酸反应生成硫酸铵和水,反应的化学方程式是2NH3•H2O+H2SO4═(NH4)2SO4+2H20;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
(5)碳酸氢铵和稀盐酸反应生成氯化铵、水和二氧化碳,反应的化学方程式是NH4HCO3+HCl═NH4Cl+H2O+CO2↑;明显的现象是有大量气泡产生.
故答案为:(1)CaO+H2O═Ca(OH)2;放热;(2)Fe+CuSO4═FeSO4+Cu;置换反应;(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;防止加热时高锰酸钾粉末进入导管;(4)2NH3•H2O+H2SO4═(NH4)2SO4+2H20;复分解反应;(5)NH4HCO3+HCl═NH4Cl+H2O+CO2↑;有大量气泡产生.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


科目:初中化学 来源: 题型:解答题
 为了探究碳酸钠和石灰水是否恰好完全反应,某化学兴趣小组将其产物进行过滤,并对滤液进行如下探究.
为了探究碳酸钠和石灰水是否恰好完全反应,某化学兴趣小组将其产物进行过滤,并对滤液进行如下探究.| 实验操作 | 实验现象 | 试验结论 |
| ①取少量滤液于试管中,滴加过量稀盐酸 | 无气泡产生 | 猜想Ⅱ不成立 |
| ②取少量滤液于试管中,滴加Na2CO3溶液 | 有沉淀生成 | 猜想成立.反应的化学方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 每100g含有营养成分 | 糖类 | 油脂[K] | 蛋白质 | 维生素C | 钙 | 镁 | 钠[ | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 7.1mg |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  巢湖银鱼 | B. |  黄山臭桂鱼 | C. |  肥西老母鸡 | D. |  祁门猕猴桃 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
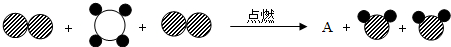
 ”表示碳原子,“
”表示碳原子,“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,该生成物A为
”表示氧原子,该生成物A为查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 待鉴别的物质 | 鉴别方法 | |
| A | 澄清石灰水和氢氧化钠溶液 | 加盐酸,观察现象 |
| B | 氯化铵固体和氢氧化钠固体 | 加熟石灰研磨,闻气味 |
| C | 生石灰和石灰石 | 加水,观察温度的变化 |
| D | 羊毛线和涤纶线 | 点燃,闻燃烧产生的气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
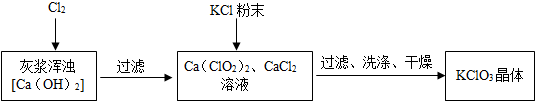
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
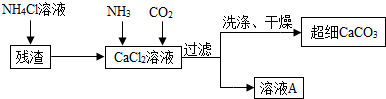
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com