
【题目】已知碳酸氢铵的化学式为NH4HCO3,计算:
(1)碳酸氢铵的相对分子质量 .
(2)碳酸氢铵中各元素的质量比 .
(3)158gNH4HCO3中含氮多少克 .
科目:初中化学 来源: 题型:
【题目】用化学用语填空。
(1)发酵粉的主要成分之一是_______(2)两个锌离子___
(3)二氧化硫中硫元素化合价_______(4)最简单的有机物___
(5)人体胃酸中的主要成分__________(6)地壳中含量最高的金属元素___
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组围绕“实验室制取氧气”进行了一系列探究活动:
(1)药品选择:下列物质中不能作为实验室制取氧气反应物的是____(填字母)。
A.水 B.过氧化氢 C.氯化钾 D.高锰酸钾(KMnO4)
(2)装置连接,所需的一些实验装置如图1所示:

仪器a的名称是____;选择气体收集方法时,气体的下列性质:A.颜色 B.可燃性 C.溶解性 D.密度,必须考虑的是__(填字母);要制取并收集一瓶干燥的氧气,所选装置的连接顺序为__(填装置字母序号)。
(3)实验探究:如图2所示,向三支试管中分别滴加浓度相同的三种溶液,观察可见:实验①中无明显现象,实验②中产生气泡,实验③中产生气泡更快,据悉你能得出的结论是_____________________________.
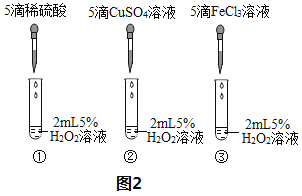
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组同学学习化学积极性高,平时喜欢收集化学用品,建立了他们自己的实验室,其实验室中部分仪器如图。
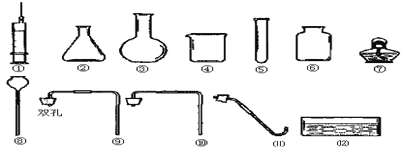
(1)写出下列仪器名称:⑤____________;⑦____________;
(2)该小组同学经过认真讨论,一致认为从二氧化碳制取原理和溶解性角度考虑,在设计制取和收集二氧化碳的装置时,一定不会选用上述仪器中的_____________。(填序号)
(3)该小组小霞同学打算选用④⑥⑾⑿三种仪器组成制取和收集氢气的装置,小红认为小霞的实验装置不能达到实验目的,你认为不能达到目的的原因是_____________________,
(4)该小组小华同学打算选用①②⑥⑨四种仪器组成制取和收集氧气的装置,若小华同学要想顺利完成实验,有两种改进方法:即仪器①用仪器_______替代,或者用仪器________替代仪器⑨。小华同学设计的装置还可以用来制取氧气,她采用的实验室制气原理为(用化学方程式表示)___________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有两种不同的原子,一种原子的原子核内有6个质子和6个中子,另一种原子的原子核内有6个质子和7个中子,则它们不相等的是( )
A.核电荷数 B.核外电子数 C.原子的带电量 D.原子的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将10%的NaOH溶液逐滴加入到20克稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示:
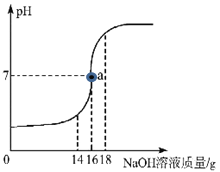
请计算:
(1)a点溶液中大量存在的离子有 。(写符号)
(2)当恰好完全反应时,消耗NaOH的质量为 克。
(3)计算稀盐酸中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋。使用时,撕去它的保护膜贴在身体上,不久便会产生热量。已知小袋中装有铁粉、碳粉和少量氯化钠。
(1)取小袋内物质,加入稀盐酸中,发生反应的化学方程式为:________。
(2)将袋内物质放在足量O2中燃烧,写出反应的化学方程式:
①____________________________、②________________。
(3)将袋内物质加入一定量的CuSO4溶液中,充分反应后过滤,滤液中的溶质一定有_____(填写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学模拟如下流程对含有大量H2SO4和CuSO4的废水进行处理,以回收金属铜,并使废水pH和重金属含量达到排放标准。
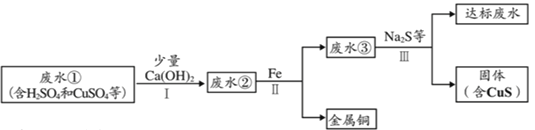
已知:步骤I无蓝色沉淀生成。
⑴Ca(OH)2的俗名为______;稀硫酸的工业用途有:______(举一例即可)。
⑵步骤Ⅱ和步骤Ⅲ都需进行的操作是______,该操作常用的玻璃仪器除玻璃棒、烧杯外,还有______;玻璃棒作用______。
⑶步骤Ⅱ得到金属铜的反应的化学方程式为______。
⑷步骤Ⅰ中加入少量Ca(OH)2最终目的是______。
⑸步骤Ⅲ需加入Na2S才能使废水达到排放标准。从微观角度看,溶液中实际发生的反应为:
Cu2+ + ______ = CuS↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com