
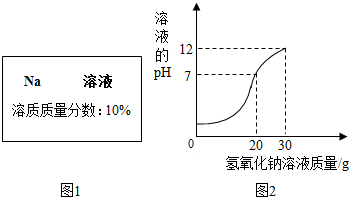
 实验室有一瓶试剂,密封完好但标签残缺(如图1所示),已知它可能是NaCl,NaOH,Na2CO3,NaHCO3中的一种.
实验室有一瓶试剂,密封完好但标签残缺(如图1所示),已知它可能是NaCl,NaOH,Na2CO3,NaHCO3中的一种.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 实验步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量气泡 | 该溶液是 化学方程式为 |
| 9.6g |
| 9.6g+100g |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 稀盐酸(或稀硫酸) | 碳酸钠溶液 Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
| 4g |
| 20g |
| 4g |
| 20g |


科目:初中化学 来源: 题型:
| A、治疗胃酸过多症 2HCl+Ca(OH)2=CaCl2+2H2O 中和反应 |
| B、铁与稀硫酸反应制氯气 2Fe+3H2SO4=Fe2(SO4)3+3H2↑ 置换反应 |
| C、雨水呈酸性的原因 CO2+H2O=H2CO3 化合反应 |
| D、吸收二氧化气体 CO2+2NaOH=Na2CO3+H2O 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
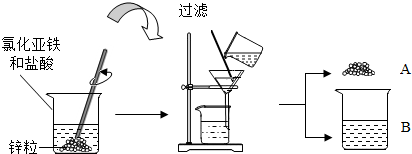
查看答案和解析>>
科目:初中化学 来源: 题型:
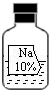 溶液不是NaNO3,为确定其成分,某同学进行如下研究.
溶液不是NaNO3,为确定其成分,某同学进行如下研究.| 实验步骤 | 步骤一 | 步骤二 | 步骤三 |
| 实验过程 | 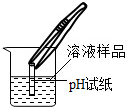 | 用洁净的铂丝蘸取该溶液放在火焰上,观察 | 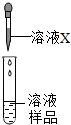 |
| 实验现象 | 试纸变色,对照色卡,pH=7 | 火焰呈黄色 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 丹丹和东东两位同学在阅读教材中的【查阅资料】草木灰的主要成分是碳酸钾,碳酸钾的化学性质和碳酸钠的化学性质相似.
丹丹和东东两位同学在阅读教材中的【查阅资料】草木灰的主要成分是碳酸钾,碳酸钾的化学性质和碳酸钠的化学性质相似.| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液于试管中, | | 猜想二成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com