
| A. | 属于有机化合物 | |
| B. | 一个帕拉米韦分子中含2个氧分子 | |
| C. | C、H、N、O四种元素的质量比为15:28:4:4 | |
| D. | 组成元素中,氢元素质量分数最大 |
分析 A、根据帕拉米韦的化学式为C15H28N4O4结合有机物的概念分析;
B、根据每个帕拉米韦分子的构成进行分析解答;
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
D、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答
解答 解:A、含有碳元素的化合物属于有机化合物,根据帕拉米韦的化学式C15H28N4O4可知它是由碳、氢、氮、氧四种元素组成的,属于有机化合物,故说法正确;
B、分子是由原子构成的,每个帕拉米韦分子是由15个碳原子、28个氢原子、4个氮原子和4个氧原子构成的,帕拉米韦分子中不含氧分子,故说法错误;
C、帕拉米韦中C、H、N、O元素质量比为(12×15):(1×28):(14×4):(16×4)=45:7:14:16,不等于原子个数比,故说法错误;
D、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%可知,帕拉米韦的相对分子质量一定,哪种元素的相对原子质量之和最大,哪种元素的质量分数最大,碳元素的相对原子质量之和为12×15=180,氢元素的相对原子质量之和为1×28=28,氮元素的相对原子质量之和为14×4=56,氧元素的相对原子质量之和为16×4=64,因此碳元素质量分数最大,故说法错误.
故选A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | SO2是组成空气的主要气体之一 | |
| B. | SO2分子中含有氧分子 | |
| C. | SO2中硫元素和氧元素的质量比为1:2 | |
| D. | SO2中硫元素的质量分数为50% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 中子数为6 | B. | 质子数为6 | ||
| C. | 电子数为6 | D. | 质子数和中子数之和是14 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | NaCl溶液 | Na2CO3 | 加入稀盐酸至不再产生气泡 |
| B | CuO粉末 | C | 加入过量稀盐酸,充分反应 |
| C | MnO2 | KCl | 溶解、过滤、蒸发结晶 |
| D | KCl溶液 | CuCl2 | 加入氢氧化钠溶液至不再产生沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
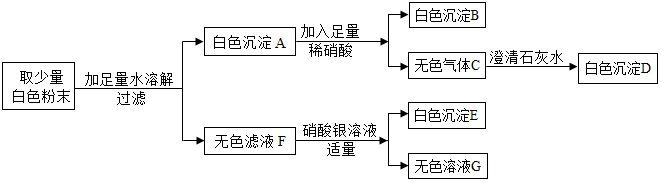
| A. | 原混合物中一定不含CuSO4,一定含有Ba(NO3)2、BaSO4、Na2CO3 | |
| B. | 白色沉淀A中含有BaCO3和BaSO4 | |
| C. | 确定原固体混合物中是否有KCl可取白色沉淀E加入足量稀硝酸,观察沉淀是否溶解 | |
| D. | 无色溶液F中最少有4种离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com