
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  |  |  | |
| A. | 4种物质均由分子构成 | B. | 反应前后各元素化合价均发生改变 | ||
| C. | 4种物质中属于氧化物的是A、B、C | D. | C、D两种物质的质量比为22:7 |
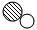
分析 根据微观示意图及各物质的分子构成可知,该反应的化学方程式可表示为2CO+2NO═2CO2+N2,据此进行判断.
解答 解:由微观示意图可知,该反应的化学方程式可表示为2CO+2NO═2CO2+N2.
A、由四种物质的分子结构模拟图,4种物质均由分子构成,故该说法正确;
B、该反应有单质生成,一定有化合价的变化,故该说法错误;
C、4种物质中A、B、C三种物质都两种元素组成且含氧元素的氧化物,故该说法正确;
D、根据反应的化学方程式,生成物C、D两种物质的质量比=(2×44):28=22:7,故该说法正确.
答案:B.
点评 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:初中化学 来源: 题型:选择题
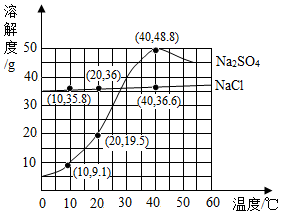 如图为Na2SO4和NaCl的溶解度曲线.下列叙述正确的是( )
如图为Na2SO4和NaCl的溶解度曲线.下列叙述正确的是( )| A. | ③④ | B. | ①② | C. | ①③④ | D. | ②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
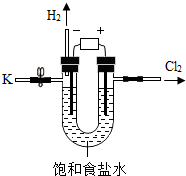 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分溶液作为待测液进行如下探究.(提示:可以忽略其他可能发生的反应对以下实验的影响;Mg(OH)2在水中不溶)
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分溶液作为待测液进行如下探究.(提示:可以忽略其他可能发生的反应对以下实验的影响;Mg(OH)2在水中不溶)
| 加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
| 烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl | B. | Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论与解释 |
| ①向白醋滴入紫色石蕊 | 观察到溶液变红 | 白醋显酸性 |
| ②向镁粉中滴加白醋直至过量 | 镁条表面有大量气泡 | 白醋能与活泼金属反应 |
| ③将白醋滴加到碳酸钙表面 | 碳酸钙表面有气泡 | 反应的化学方程式是CaCO3+2CH3COOH═Ca(CH3COO)2+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

 ,属于非金属元素(填“金属”或“非金属”),它在化学反应中易得(填“得”或“失”)电子,变成S2-(填离子符号).由此可见,元素的化学性质与原子结构中的最外层电子数关系密切.
,属于非金属元素(填“金属”或“非金属”),它在化学反应中易得(填“得”或“失”)电子,变成S2-(填离子符号).由此可见,元素的化学性质与原子结构中的最外层电子数关系密切.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用硫在密闭容器中燃烧,除去密闭容器内空气中的氧气 | |
| B. | 向某未知溶液中加入 AgNO3 溶液,产生白色沉淀,证明溶液是盐酸 | |
| C. | 按溶解、过滤、蒸发的操作顺序可以分离 CaCl2、CaCO3 的混合物 | |
| D. | 将 pH 试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
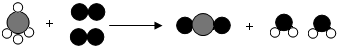
| A. | 示意图中的各物质均属化合物 | |
| B. | 化学反应的本质是原子间的分离与重新组合过程 | |
| C. | 分子是由原子构成的 | |
| D. | 化学反应前后原子数目没有变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com