
分析 (1)根据质量守恒定律可知生成二氧化碳的质量;(2)根据二氧化碳的质量计算出与碳酸钠反应的氯化氢的质量,用氯化氢的质量除以与碳酸钠反应的盐酸的质量;根据二氧化碳的质量算出碳酸钠的质量,再用碳酸钠的质量除以废水的质量乘以百分之百.
解答 解:(1)由质量守恒定律可知生成二氧化碳的质量为:100g+37g-132.g=4.4g;
(2)设生成4.4g二氧化碳需要碳酸钠的质量为X,消耗氯化氢的质量为Y则:
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
X Y 4.4g
根据:$\frac{106}{x}=\frac{73}{y}=\frac{44}{4.4g}$
解得X=10.6g,
解得Y=7.3g
废水中Na2CO3的质量分数:$\frac{10.6g}{100g}$×100%=10.6%;
所用稀盐酸溶质的质量分数:$\frac{7.3g}{153g-80g}$×100%=10%.
答:废水中Na2CO3的质量分数是10.6%,所用稀盐酸溶质的质量分数为10%.
点评 本题容易出错的地方是计算盐酸的质量分数时,根据二氧化碳算出的氯化氢不能除以总盐酸的质量,由图示可知与碳酸钠反应消耗的盐酸质量为:153g-80g=73g.


科目:初中化学 来源: 题型:填空题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | MnO2(KCl)加水溶解、过滤、蒸发、结晶 | |
| B. | KCl(K2CO3)加足量稀硫酸、过滤、蒸发、结晶 | |
| C. | CuO(Cu)加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | BaSO4(BaCO3)加足量稀盐酸、过滤、洗涤、干燥 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
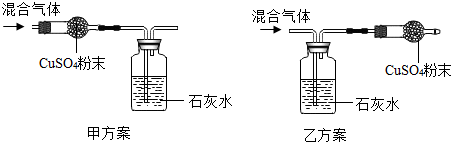
| A. | 甲、乙两方案都能证明原混合气体中是否含有CO2和H2O | |
| B. | 乙方案无法证明原混合气体中是否含有H2O,只能证明是否含有CO2 | |
| C. | 甲方案无法证明原混合气体中是否含有CO2,只能证明是否含有H2O | |
| D. | 甲、乙两种方案都无法证明原混合物中是否含有CO2和H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
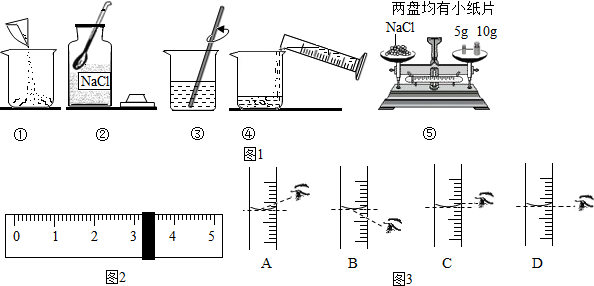
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
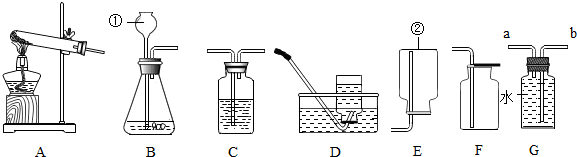
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验操作 | 实验现象 | 实验结论 |
| 将步骤三B试管中溶液倒入盛有锌粒的试管中 | 有气泡产生 | 猜想一正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com