

| CO32- | HCO3- | OH- | |
| Ba2+ | 不溶 | 溶 | 溶 |
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取该NaOH溶液,加入过量BaCl2溶液 | 产生白色沉淀 | 证明猜想1、5不成立(填数字) |
| 步骤2 | 取步骤1中上层清液,滴加稀盐酸 | 无气泡产生 | 证明原溶液不含HC${{O}_{3}}^{-}$(填“离子”) |
| 步骤3 | 另取步骤1中上层清液,滴加酚酞 | 溶液未变红 | 证明原溶液不含OH-(填“离子”) |
分析 (1)①根据碳酸根离子和钙离子、钡离子会生成碳酸钙沉淀、碳酸钡沉淀,硫酸和氢氧化钠、碳酸钠会生成硫酸钠进行分析;
②根据蒸发、过滤过程中需要的玻璃仪器进行分析;
③根据氯化钠在通电的条件下生成钠和氯气进行分析;
(2)根据氯化钠溶液在通电的条件下生成氢氧化钠、氯气和氢气,然后依据质量守恒定律进行配平;
(3)【提出猜想】根据二氧化碳和氢氧化钠的反应生成物进行猜想;
【实验验证】根据碳酸根离子和钡离子会生成碳酸钡沉淀,根据碳酸根离子、碳酸氢根离子和酸反应生成二氧化碳气体,氢氧根离子能使酚酞变红色进行分析;
【实验结论】根据前面的实验得出正确的结论.
解答 解:(1)①碳酸根离子和钙离子、钡离子会生成碳酸钙沉淀、碳酸钡沉淀,所以加入过量Na2CO3溶液目的是除去CaCl2和氯化钡,硫酸和氢氧化钠、碳酸钠会生成硫酸钠,所以不能用过量稀硫酸代替过量稀盐酸的原因是会生成新的杂质硫酸钠;
②蒸发过程中用到的玻璃仪器有玻璃棒、酒精灯,过滤过程中用到的玻璃仪器有烧杯、漏斗、玻璃棒,所以两步操作中需要的玻璃仪器有玻璃棒;
③氯化钠在通电的条件下生成钠和氯气,化学方程式为:2NaCl$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑;
(2)氯化钠溶液在通电的条件下生成氢氧化钠、氯气和氢气,然后依据质量守恒定律进行配平,化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(3)【提出猜想】二氧化碳和氢氧化钠的反应为:2NaOH+CO2═Na2CO3+H2O;Na2CO3+CO2+H2O═2NaHCO3
NaOH+NaHCO3═Na2CO3+H2O,所以猜想2:含有氢氧化钠、碳酸钠,猜想4:碳酸氢钠、碳酸钠;
【实验验证】碳酸根离子和钡离子会生成碳酸钡沉淀,根据碳酸根离子、碳酸氢根离子和酸反应生成二氧化碳气体,氢氧根离子能使酚酞变红色,所以
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取该NaOH溶液,加入过量BaCl2溶液 | 产生白色沉淀 | 证明猜想1、5不成立(填数字) |
| 步骤2 | 取步骤1中上层清液,滴加稀盐酸 | 无气泡产生 | 证明原溶液不含HC${{O}_{3}}^{-}$、(填“离子”) |
| 步骤3 | 另取步骤1中上层清液,滴加酚酞 | 溶液未变红 | 证明原溶液不含OH-(填“离子”) |
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 1、5 | ||
| 步骤2 | 稀盐酸 | HC${{O}_{3}}^{-}$、 | |
| 步骤3 | 酚酞 | OH- |
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧产生大量白色气体 | |
| B. | 铁丝在氧气中燃烧,产生白色火焰,生成一种黑色固体 | |
| C. | 镁带燃烧,发出耀眼强光.生成一种白色固体 | |
| D. | 硫在空气中燃烧,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16.6% | B. | 6.1% | C. | 12.2% | D. | 9.1% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D |
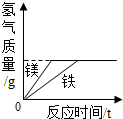 |  |  |  |
| 常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | 敞口放置于空气中的浓硫酸或稀盐酸 | 加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | 少量的碳在密闭的集气瓶中与氧气完全燃烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 单质是由同种元素组成的,所以只含一种元素的物质一定是单质 | |
| B. | 草木灰和碳酸氢铵是常用的肥料,所以将二者混合施用,可增加肥效 | |
| C. | CO2和CO都是碳的氧化物,所以它们的化学性质相似 | |
| D. | 在氯化钠溶液中有Na+和Cl-,所以氯化钠溶液能导电 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 植树绿化,美化环境 | B. | 提倡绿色出行,发展公共交通 | ||
| C. | 外出时佩戴防雾霾口罩 | D. | 减少燃烧发电,增加太阳能发电 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com