(1)将扭成螺旋状的光亮铜丝,用酒精灯烧红后,立即插入氧气瓶中,冷却后铜丝表面变黑,化学方程式为 ______.此时铜丝发生了 ______反应(填:“氧化”或“还原”).(2)再将上述铜丝加热,立即伸入氢气瓶中,冷却后铜表面 ______.此时氢气发生了 ______反应(填:“氧化”或“还原”),化学方程式为 ______.经过两次实验后,铜丝的质量 ______(填“不变”“增大”或“减小”).
解:(1)铜与氧气发生反应,生成黑色的氧化铜,铜丝得氧,发生氧化反应;故化学方程式为

;
(2)热的氧化铜与氢气发生反应,被还原,变回光亮铜丝,氢气铜丝得氧,发生氧化反应,而整个过程铜丝的质量不变,故化学方程式为
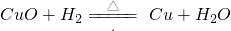
故答为:(1)

,氧化;
(2)光亮红色,氧化,

,不变
分析:(1)将扭成螺旋状的光亮铜丝,用酒精灯烧红后,立即插入氧气瓶中,冷却后铜丝表面变黑,铜与氧气发生反应,生成黑色的氧化铜,铜丝得氧,发生氧化反应;
(2)热的氧化铜与氢气发生反应,被还原,变回光亮铜丝,氢气铜丝得氧,发生氧化反应;根据质量守恒定律可知,整个过程铜丝的质量不变.
点评:由题目中的信息,结合课本知识,根据质量守恒定律,正确书写有关的化学方程式;掌握氧化反应和还原反应的概念与应用.

 ;
;
 ,氧化;
,氧化; ,不变
,不变

 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案