
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量滤液于试管中,向其滴加2滴~3滴无色酚酞试液,振荡 | 溶液由无色变为红色 | 该瓶中白色粉末一定不是碳酸钙和氯化钠 |
| (2)另取少量滤液于试管中,滴加过量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 该瓶中白色粉末一定有碳酸钠,涉及的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓ |
分析 【实验Ⅱ】根据碳酸钠在水中的溶解度较小,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
【实验Ⅲ】根据碱性溶液能使酚酞显红色,碳酸钠和氯化钙会生成碳酸钙沉淀和氯化钠进行分析;
【反思与交流】根据氢氧化钠和二氧化碳反应会生成碳酸钠和水进行分析.
【实际应用】洗涤后溶液呈中性说明恰好完全反应,根据反应的化学方程式,由反应所消耗的氢氧化钠的质量计算出石油产品中硫酸的质量.
解答 解:【实验Ⅱ】小明取实验Ⅰ得到的固体于试管中,滴加足量稀盐酸后,观察到有有气泡产生,于是小明马上就得出结论,该瓶中白色粉末一定是碳酸钙,但是小军却认为小明的结论不一定正确,固体还可能是碳酸钠,因为碳酸钠在水中的溶解度较小,碳酸钠量较多时,也会出现不溶性固体,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
【实验Ⅲ】碱性溶液能使酚酞显红色,碳酸钠和氯化钙会生成碳酸钙沉淀和氯化钠,所以
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量滤液于试管中,向其滴加2滴~3滴无色酚酞试液,振荡 | 溶液由无色变为红色 | 该瓶中白色粉末一定不是碳酸钙和氯化钠 |
| (2)另取少量滤液于试管中,滴加过量氯化钙溶液,振荡,静置 | 产生白色沉淀 | 该瓶中白色粉末一定有碳酸钠,涉及的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| 实验步骤 | 实验现象 | 实验结论 |
| 碳酸钙和氯化钠 | ||
| 产生白色沉淀 | Na2CO3+CaCl2=2NaCl+CaCO3↓ |
点评 本题考查的是残缺标签瓶内成分的实验探究,完成此题,可以依据学过的知识结合物质的性质进行.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
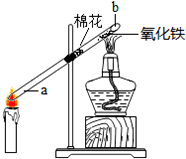 化学兴趣小组在老师指导下,对“蜡烛燃烧的产物”进行探究.
化学兴趣小组在老师指导下,对“蜡烛燃烧的产物”进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 粘合剂 | B. | 制冷剂 | C. | 防腐剂 | D. | 催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
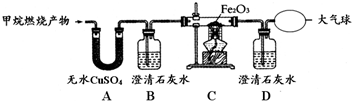
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
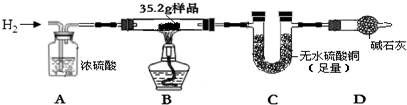
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com