
分析 (1)根据化学反应前后原子的种类和数目不变进行解答;
(2)根据大量排放出的二氧化硫能形成酸雨以及氨水呈碱性,pH大于7进行解答;
(3)根据溶液配制的仪器进行解答;
(4)根据氧化铁与盐酸的反应写出反应的化学方程式.
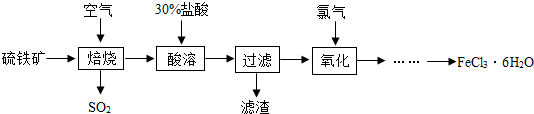
解答 解:(1)由化学反应前后原子的种类和数目不变,4FeS2+11X═2Fe2O3+8SO2可知,X的化学式为O2;
(2)大量排放出的二氧化硫能形成酸雨;氨水呈碱性,pH大于7;
(3)在实验室中,欲用38%(密度为1.18g/mL)的盐酸配制30%的盐酸,则需要的玻璃仪器主要有量筒、烧杯、玻璃棒;
(4)氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,该反应符合复分解反应的条件,属于复分解反应.
故答案为:(1)O2;
(2)酸雨,大于;
(3)量筒,烧杯;
(4)Fe2O3+6HCl═2FeCl3+3H2O,复分解.
点评 本题重点考查了化学方程式的书写,熟悉常用酸碱的性质,难道较小.


科目:初中化学 来源: 题型:解答题
| 实验步骤 | a | b | c |
 | 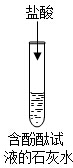 | 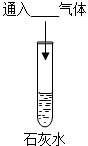 | |
| 现象 | 溶液变为蓝色 | 溶液由红色变成无色 | 有白色沉淀生成 |
| 结论 | 氢氧化钙溶液能与酸碱指示剂作用 | 反应的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O氢氧化钙能与酸反应 | 氢氧化钙能与酸性氧化物(填物质类别)反应 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 1.用药匙尾端挑一点氢氧化钙粉末,分别加入A、B两支试管中,各加1mL水振荡 | 两试管中液体均呈白色浑浊状态 | 不填 |
| 2.在A试管中再加少量水振荡试管;向B试管中加入少量浓盐酸,振荡试管 | A试管中液体仍然呈白色浑浊状态.B试管中 白色浑浊消失成为无色溶液 | 氢氧化钙难溶于水;氢氧化钙能与盐酸反应生成易溶物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 汽油和洗涤剂除油污的原理相同 | |
| B. | 空气、糖水、高锰酸钾都属于混合物 | |
| C. | 纯碱、烧碱都属于碱 | |
| D. | 只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 如果合金为锌和铁,m可能是0.2g | |
| B. | 反应后溶液中的溶质只有两种 | |
| C. | 如果合金为锌和镁,m可能是0.1g,则该合金中锌的质量分数为50% | |
| D. | 如果合金为锌和铁,所加稀盐酸溶质质量分数一定大于7.3% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
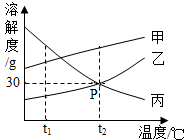 甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 常用于淡化海水的方法有蒸馏法、过滤法等 | |
| B. | 粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发 | |
| C. | 通常在苦卤中加入熟石灰制取氢氧化镁 | |
| D. | 海水中的食盐用途广泛,例如侯德榜利用食盐为原料制得了纯碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com