
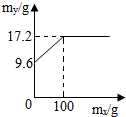
 让我们与小松同学一起参与以下探究:
让我们与小松同学一起参与以下探究:| 样 品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
| 54 |
| x |
| 6 |
| 1.0g |
| 340 |
| 100g?w% |
| 152 |
| 7.6g |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:
| A、HCl、Na2SO4、KCl |
| B、MgCl2、HNO3、AgNO3 |
| C、NaCl、BaCO3、KNO3 |
| D、CuSO4、KOH、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:
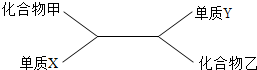 根据下列化合物与单质相互转化的关系回答:
根据下列化合物与单质相互转化的关系回答:查看答案和解析>>
科目:初中化学 来源: 题型:
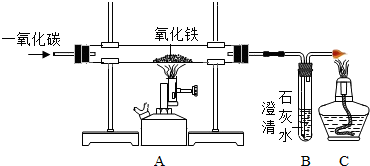
查看答案和解析>>
科目:初中化学 来源: 题型:
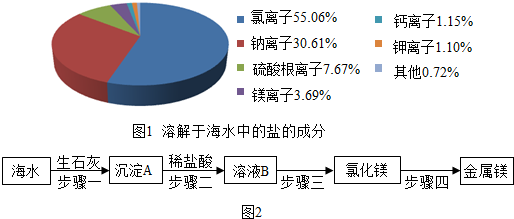
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 元素名称 | 氢 | 碳 | 氧 | 铁 |
| 元素符号 | H | C | O | Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com