
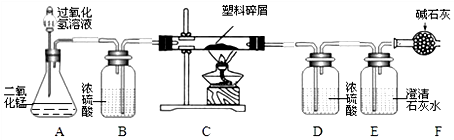
分析 (1)按上面连接好装置,在装入药品之前,必须检查装置气密性;
(2)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;
(3)塑料袋试样中含有碳元素和氢元素,完全燃烧生成水和二氧化碳,水能被浓硫酸吸收,二氧化碳能使澄清石灰水变浑浊;
(4)塑料袋试样中的氢元素完全燃烧后全部转化到水中,水中的氢元素质量即为塑料袋试样中氢元素的质量;
(5)若装置中没有连接装置B,将使测定生成的水的质量偏大,从而导致该塑料试样中氢元素的质量测算结果偏大.
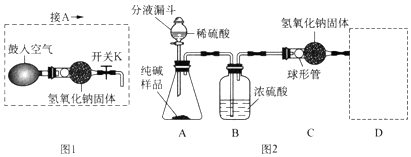
解答 解:(1)按上面连接好装置,在装入药品之前,必须进行的操作是检查装置气密性.
故填:检查装置气密性.
(2)装置E中,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
(3)判断塑料袋试样中含有碳元素的依据是E装置中澄清石灰水变浑浊,这是因为澄清石灰水变浑浊,说明反应生成了二氧化碳,进一步说明样品中含有碳元素;
装置F的作用是:防止空气中的二氧化碳进入E中使测量结果不准确.
故填:E装置中澄清石灰水变浑浊;防止空气中的二氧化碳进入E中使测量结果不准确.
(4)该塑料袋试样中氢元素的质量为:5.4g×$\frac{2}{18}$×100%=0.6g,
故填:0.6g.
(5)若装置中没有连接装置B,将使测定生成的水的质量偏大,从而导致该塑料试样中氢元素的质量测算结果偏大.
故填:偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 生活中用镶有金刚石的玻璃刀裁划玻璃 | |
| B. | 常温下的超导体可广泛用于输电导线 | |
| C. | 农业上常用熟石灰改良酸性土壤 | |
| D. | 液态二氧化碳灭火器用于扑灭图书、档案的失火 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
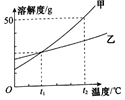
| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯乙 | |
| C. | t2℃时,将甲和乙两种物质的溶液分别降温到t1℃,析出晶体的质量甲一定大于乙 | |
| D. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤液中一定有Zn2+和Cu2+ | |
| B. | 滤液中一定有Zn2+,可能有Cu2+和Ag+ | |
| C. | 滤渣中一定有Cu | |
| D. | 滤渣中一定是Cu和Ag的混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com