
 Mg+Cl2↑.
Mg+Cl2↑. Mg+Cl2↑.
Mg+Cl2↑.

科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
(7分)海水又苦又咸,是因为其中含有大量的Na+、Cl-和一些Mg2+、Ca2+、SO42- 等。目前世界上60%的镁是从海水中提取的,其主要步骤如下:
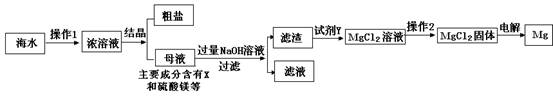
请根据流程图回答:
1.操作2的名称是 ,试剂Y显酸性,它是 ;
2.母液中的X是 ,请写出母液中含有的微粒 ;
3.氯化镁固体的电解属分解反应,写出该反应的化学方程式: 。
查看答案和解析>>
科目:初中化学 来源:2010年广东省广州市萝岗区中考化学一模试卷(解析版) 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com