
 节假日双休日,去野炊实为一大快事.如果遇到下面一些问题,你该如何处理?
节假日双休日,去野炊实为一大快事.如果遇到下面一些问题,你该如何处理?分析 (1)根据生活实际,导热性好的材料是金属;
(2)根据小卵石的作用是过滤其中的某些大的不溶性杂质分析回答.
(3)根据溶液的特征分析回答;
(4)根据化合价原则求出元素的化合价;
(5)根据洗洁精能乳化油污分析回答;
(6)根据燃烧的条件进行分析解答.
解答 解:(1)金属材料坚硬、结实,而无机非金属材料如陶瓷、玻璃等硬而脆易破碎;因此,应携带导热性好,不易破碎的金属材料制成的餐具;
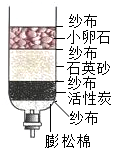
(2)将浑浊的河水用如图所示的简易净水器进行净化,其中其中小卵石、石英砂的作用是过滤其中的某些不溶性杂质;
(3)因为溶液的特征具有均一性、稳定性,故取少量汤进行品尝就可知道整锅汤盐味如何;
(4)根据在化合物中正负化合价代数和为零,铬酸铅中铅元素的化合价为+2价,氧元素化合价为-2,则PbCrO4中铬元素(Cr)的化合价为:(+2)+x+(-2)×4=0,解得x=+6;
(5)洗洁精具有乳化作用,所以同学们用洗洁精将油腻的碗筷洗得干干净净,这是利用了洗洁精的乳化作用,使油脂以细小油滴悬浮于水中而洗净餐具;
(6)促进可燃物燃烧的条件有两个:增大可燃物与氧气的接触面积,增大氧气浓度,迅速往“灶”里塞满枯枝,进入的空气少,可燃物与氧气的接触面积小了,燃烧会不充分;
故答案为:(1)A;(2)过滤;(3)均一性;(4)+6;(5)乳化;(6)有充足的空气.
点评 学会把化学知识和生活实际结合起来,培养学生从题目中搜索信息的能力.化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,关乎我们的生存、健康和社会的发展,是中考热点之一.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
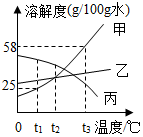 如图为甲、乙、丙三种固体物质的溶解度曲线,请据图回答:
如图为甲、乙、丙三种固体物质的溶解度曲线,请据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 现有盐酸、稀硝酸、氢氧化钙三瓶标签遗失的溶液,为了鉴别他们,小刚先将它们贴上标签,分别为A、B、C,并按如图步骤进行实验,记录相应的实验现象:
现有盐酸、稀硝酸、氢氧化钙三瓶标签遗失的溶液,为了鉴别他们,小刚先将它们贴上标签,分别为A、B、C,并按如图步骤进行实验,记录相应的实验现象:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 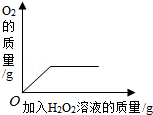 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 | |
| B. | 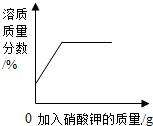 20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | |
| C. | 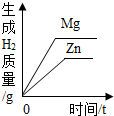 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 | |
| D. | 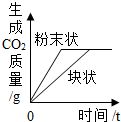 等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com