
(6分) 现有以下六种物质:硝酸钾、小苏打、铝、石墨、天然气、氮气。根据下列要求用化学式填空:
(1)可充入食品包装袋用于防腐的是 ; (2)发酵粉的主要成分之一是 ;
(3)可作干电池电极的是 ; (4)可作燃料,其主要成分是 ;
(5)其组成元素是地壳中含量最高的金属元素 ;(6)可作复合肥料的是 。
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:初中化学 来源:2014年初中毕业升学考试化学试卷(湖南省株洲市)(解析版) 题型:选择题
我市湘江风光带桥头广场上介绍侯德榜曾在株洲开办“永利化工厂”,利用联合制碱法(侯氏制碱法)生产纯碱。下列有关联合制碱法的原料(氯化钠、二氧化碳、氨气、水)与产品(碳酸钠、氯化铵)的说法不正确的是
A.碳酸钠广泛应用于玻璃、造纸、纺织和洗涤剂的生产
B.氯化钠在自然界中分布很广,海洋、盐湖、盐井、盐矿等都是氯化钠的来源
C.侯氏制碱法消耗了二氧化碳,极大地缓解了酸雨的形成
D.氯化铵与熟石灰粉末混合研磨,放出具有刺激性气味的氨气
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(湖北省武汉市)(解析版) 题型:探究题
(5分)某化学兴趣小组的同学对呼吸面具的制氧原理产生好奇心,通过查阅资料得知,呼吸面具中制取氧气的主要原料是固体过氧化钠(Na2O2)。过氧化钠分别能和二氧化碳、水反应都生成氧气,反应的化学方程式为:
2Na2O2+2H2O 4NaOH+O2↑ 2Na2O2 +2CO2
4NaOH+O2↑ 2Na2O2 +2CO2 2Na2CO3+O2
2Na2CO3+O2
为了测定呼吸面具中过氧化钠的质量分数,该小组的同学在老师的指导下,利用下图所示装置(固定装置一略去)开展探究,并得到正确的结论。
已知,装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。
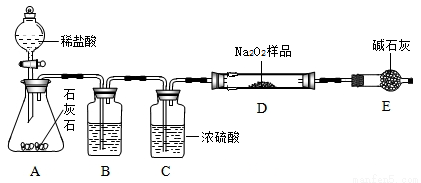
请回答下列问题:
(1)仪器a的名称是 ,装置A的作用是 ;
(2)不用装置E代替装置C的理由是 。
(3)装置D中过氧化钠药品的质量为mg,装置D在反应前后的总质量n1g和n2g。若药品中所含杂质既不溶于水也不参加化学反应,则药品中过氧化钠的质量分数 = 。
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(湖北省武汉市)(解析版) 题型:选择题
二氧化钛(TiO2)是一种用途广泛的化工原料,用四氯化钛(TiCl4)与某常见物质X反应可
制得二氧化钛,反应的化学方程式为:TiCl4 + □X = TiO2 + 4HCl 关于物质X,下列说法正确的
是( )
A.该物质由碳、氢、氧三种元素组成
B.该物质的化学式为H2O2
C.该物质中氢、氧元素的质量比为1:8
D.该物质中氧元素的质量分数是5%
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(江苏连云港市)(解析版) 题型:选择题
下列事实可用于判断X、Y两种金属的活动性顺序的是
①X能和稀盐酸反应而Y不能;②X能从Y的盐溶液中置换出Y;③常温下X能与氧气反应而Y不能;④在化合物中X显+3价,Y显+2价。
A.①② B.①②③ C.③④ D.①②④
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(江苏连云港市)(解析版) 题型:选择题
“向污染宣战”是今年我国“世界环境日”的主题。下列做法有利于保护环境的是
A.禁止吸烟 B.燃放鞭炮 C.多开汽车 D.乱扔垃圾
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(江苏省苏州市)(解析版) 题型:选择题
有关粗盐提纯的实验操作合理的是
A.溶解前用玻璃棒研磨大颗粒粗盐
B.过滤时液体的液面要低于滤纸边缘
C.加热蒸发时要不断搅拌直至水分全部蒸干
D.实验结束随即用手将蒸发皿从三角架上取下
查看答案和解析>>
科目:初中化学 来源:2014年初中毕业升学考试化学试卷(广东省广州市)(解析版) 题型:填空题
(7分)使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
 (1)镁元素在自然界中是以(填“单质”或“化合物”)形式存在。
(1)镁元素在自然界中是以(填“单质”或“化合物”)形式存在。
(2)工业制镁的一种原理是2MgO+Si+2CaO ====== 2Mg↑+Ca2SiO4,抽走容器中的空气对反应有促进作用,且能防止空气中的物质与Mg反应使产品混有 (填化学式)。
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g 。
①步骤2中Mg(OH)2分解的化学方程式为。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m=g。
③分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O==Ca(OH)2;Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓;。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com