
 请用所学化学知识解释下列原理.
请用所学化学知识解释下列原理.分析 (1)根据盐酸具有挥发性,所以制取的二氧化碳常有混有氯化氢气体进行分析;
(2)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠进行分析;
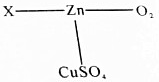
(3)根据金属会与氧气、盐、酸等物质发生反应,锌和氧气反应生成氧化锌,金属和酸反应生成盐和水进行分析.
解答 解:(1)盐酸具有挥发性,所以制取的二氧化碳常有混有氯化氢气体而具有刺激性气味;
(2)碳酸钙在高温的条件下生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)金属会与氧气、盐、酸等物质发生反应,所以X可能是盐酸,锌和氧气反应生成氧化锌,锌和盐酸反应生成氯化锌和氢气,化学方程式为:2HCl+Zn=ZnCl2+H2↑,2Zn+O2$\frac{\underline{\;\;△\;\;}}{\;}$2ZnO.
故答案为:(1)挥发;
(2)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)HCl,2HCl+Zn=ZnCl2+H2↑,2Zn+O2$\frac{\underline{\;\;△\;\;}}{\;}$2ZnO.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 溶液中溶质的质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/mL | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/g/mL | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2+H2SO4═BaSO4↓+2HCl | B. | Mg(OH)2+2HCl=MgCl2+2H2O | ||
| C. | CuO+H2SO4=CuSO4+H2O | D. | SO2+2NaOH=Na2SO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小明同学采用如图装置用双氧水制取并收集80毫升O2,其中弹簧夹可控制气体在导管中流通或阻断.仔细如图,(甲、丙装置中均为纯水,乙锥形瓶内黑色颗粒为MnO2).请回答:
小明同学采用如图装置用双氧水制取并收集80毫升O2,其中弹簧夹可控制气体在导管中流通或阻断.仔细如图,(甲、丙装置中均为纯水,乙锥形瓶内黑色颗粒为MnO2).请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③ | B. | ①④ | C. | ①② | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com