
【题目】“队员”硫酸,走进了有许多“食人兽”(即能与硫酸发生反应的物质)的小山,请你帮助它走出小山.
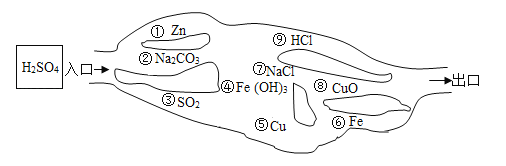
(1)请用图中物质前的序号连接起来表示所走的路线:
入口→______→______→______→______→出口.
(2)小山中潜伏着红褐色与黑色的“食人兽”,若硫酸遇上,发生的反应方程式为:____,___.
【答案】③ ⑤ ⑦ ⑨ 2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O CuO+H2SO4=CuSO4+H2O
【解析】
(1)因为硫酸不能和非金属氧化物二氧化硫、不活泼金属铜、氯化钠、盐酸反应,所以正确路线是③ ⑤ ⑦ ⑨,故填:③;⑤; ⑦;⑨。
(2)氢氧化铁红褐色和硫酸反应生成硫酸铁和水化学方程式为2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O 氧化铜是黑色,和硫酸反应生成硫酸铜和水,化学方程式为CuO+H2SO4=CuSO4+H2O,故填: 2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O ; CuO+H2SO4=CuSO4+H2O。


科目:初中化学 来源: 题型:
【题目】如图1是实验室常用气体制备装置,据图回答问题:
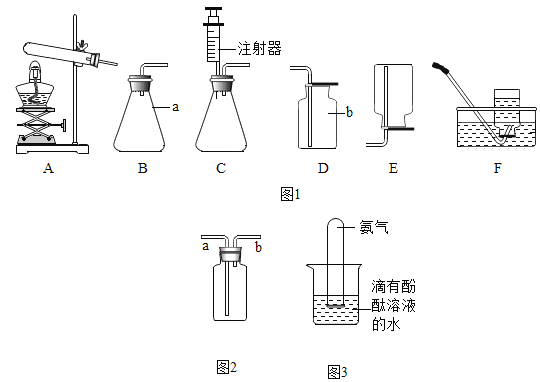
(1)请写出指定仪器的名称:a_____,b_____;
(2)实验室用高锰酸钾制氧气的化学方程式是_____,应选择的发生装置是_____(填字母代号),如果选用图2装置收集氧气,气体应从_____(填“a”或“b”)端导入;
(3)某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气,写出此反应的化学方程式_____;实验中,同学们发现不能得到平稳的氧气流,大家提出从两个方面加以改进:
一是把发生装置由B改为C,其理由是_____;
二是将过氧化氢溶液加水稀释,溶液的稀释需要经过计算、量取、混匀三个步骤,如果把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,需加水的质量为_____g,在稀释过程中,除了烧杯外,还需要用到的仪器有_____(填数字序号);
①量筒 ②药匙 ③试管 ④酒精灯 ⑤滴管 ⑥玻璃棒
(4)实验室可用加热氯化铵和熟石灰的固体混合物制取氨气(NH3)。
①制取氨气应选用的装置是_____(填字母代号);
②氨气极易溶于水,氨水显碱性。则图3实验可观察到什么现象?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙同学在学完酸的化学性质后,做了如下图的实验。
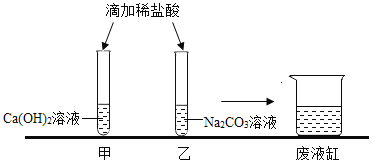
实验结束后,甲、乙同学依次将废液缓慢倒入同一洁净的废液缸中,然后进行了讨论。
(讨论1)甲做实验时没有观察到明显现象,所以对Ca(OH)2和稀盐酸能否发生反应提出质疑。乙认为甲的实验设计有问题。应当先____________________,再滴加稀盐酸就可以看到发生反应。
(讨论2)乙向废液缸内缓慢倾倒液体时观察到废液缸中先产生气泡。后出现白色沉淀。据此判断甲中的废液中含有的溶质是______________,乙的废液中含有的溶质是_____________________。
(1)为了科学处理实验后产生的废液。他们对废液缸中最终废液的成分进行探究。
(提出问题)最终废液中含有的溶质是什么?
(猜想与假设)甲: NaCl 和CaCl2; 乙: NaCl 和Na2CO3
(活动与探究)甲、乙同学为了验证自己的猜想分别取少量废液于试管中。
甲:向其中滴加Na2CO3溶液,无明显现象。结论:甲猜想不成立。 乙猜想成立。
乙:向其中滴加CaCl2溶液,出现白色沉淀。结论:_____________________________。
(表达与交流) (1)处理该废液的方法是_________________________。
(2)要想证明Ca(OH)2和稀盐酸能发生反应,还可以采用的方法是:在两只试管中加入等质量的一药匙Ca(OH)2固体,_________________________,会看到_________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是三种物质的溶解度曲线.下列说法错误的是( )
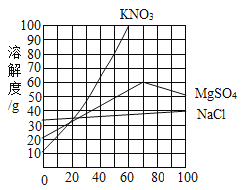
A.升高温度,可以使三种物质的溶解度增大
B.降低温度.可以除去饱和KNO3溶液中含有的少量NaCl
C.50℃时,三种物质的溶解度由大到小的顺序是:KNO3>MSO4>NaCl
D.50℃时,三种饱和溶液降温至10℃,所得溶液溶质的质量分数由大到小的顺序是:NaCl>MgSO4>KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宝钢湛江钢铁基地项目位于湛江市东海岛,2015年11月一号高炉点火生产钢铁。在炼铁工业中,常用石灰石将铁矿石中的杂质二氧化硅转化为炉渣除去,发生反应的化学方程式为:CaCO3+SiO2![]() X+CO2↑,其中X的化学式是( )
X+CO2↑,其中X的化学式是( )
A. CaSiO4B. Ca2SiO3C. CaSi2O3D. CaSiO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国女科学家屠呦呦发现青蒿素,并于2015年获得诺贝尔医学奖.已知青蒿素的化学式为C15H2205,它是一种用于治疗疟疾的药物.
(1)青蒿素分子由_____种元素构成,一个青蒿素分子含有_____个原子.
(2)青蒿素分子中C、H、O三种元素的质量比为_____.
(3)24g青蒿素中所碳元素的质量为_____ g.(计算结果精确到一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂有甲、乙两个车间,它们排放的废水中均含三种离子,经分析这些离子是Ba2+、Cu2+、K+、NO3﹣、SO42﹣、CO32﹣。甲车间废水呈碱性,若将甲、乙车间的废水按适当比例混合,使废水中的某些离子恰好完全反应转化为沉淀(如图所示)。下列分析正确的是( )
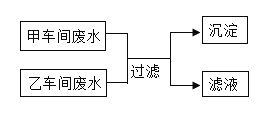
A.甲车间的废水含有的离子是K+、CO32﹣、NO3﹣
B.图中的沉淀是硫酸钡和碳酸钡
C.图中滤液所含阳离子与阴离子的数目比为1:1
D.若向乙车间的废水中加入适量铁粉,充分反应后过滤,滤液可直接排放
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂。以下是由废铜料(含铁)生产硫酸铜晶体的流程。

(1) B的化学式为________,操作a的名称是________。
(2)②的反应基本类型为___________;反应①、③的化学方程式分别为①______________;③______________。
(3)已知:![]() 从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和_______________。
从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁生锈造成金属资源浪费,但将颗粒极小的铁粉添加进燕麦中,不但起到干燥和延缓食品变质的作用,还可作为补铁剂。请用化学用语回答:
(1)铁锈主要成分氧化铁的化学式为_______;
(2)铁粉吸收水分,标出水中氢元素的化合价________;
(3)铁粉与胃酸反应生成的亚铁离子的离子符号为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com