
 已知:①CO2+H2O+Na2CO3=2NaHCO3;
已知:①CO2+H2O+Na2CO3=2NaHCO3;| 物质 | 碳酸钠 | 碳酸氢钠 | 氢氧化钠 |
| 溶解度 | 21.8g | 9.6g | 109.0g |
分析 (1)根据实验室用盐酸和碳酸钙反应制取二氧化碳时,盐酸应该通过长颈漏斗添加到相应的反应器中,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,饱和碳酸氢钠会吸收氯化氢,浓硫酸有吸水性进行分析;
(2)根据碳酸钠和水、二氧化碳反应生成碳酸氢钠,依据碳酸钠的质量进行计算.
解答 解:(1)实验室用盐酸和碳酸钙反应制取二氧化碳时,盐酸应该通过长颈漏斗添加到相应的反应器中,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+CO2+H2O,饱和碳酸氢钠会吸收氯化氢,浓硫酸有吸水性,所以为得到纯净、干燥的CO2气体,应先将混合气体通过盛有C的洗涤装置,然后,再将气体通过盛有E的洗涤装置;
(2)设反应会生成碳酸氢钠的质量为x,消耗水的质量为y
CO2+H2O+Na2CO3=2NaHCO3,
18 106 168
y 100g×13.25% x
$\frac{106}{100g×13.25%}$=$\frac{168}{x}$$\frac{18}{y}$
x=21g
y=2.25g
设溶液中含有碳酸氢钠的质量为z
100g:9.6g=[100g×(1-13.25%)-2.25g]:z
z=8.112g
所以最后所得溶液中碳酸氢钠的质量为:8.112g+84.5g=92.6g.
故答案为:(1)长颈漏斗,CaCO3+2HCl=CaCl2+CO2+H2O,C,E;
(2)21g,92.6g.
点评 本题主要考查了实验室制取二氧化碳的相关知识和溶解度计算的知识,难度不大,注意解题的规范性和准确性.


科目:初中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④①③② | C. | ③①④② | D. | ①②④③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入足量氯化钙溶液; | 白色沉淀产生 | 该反应的化学方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| (2)将上述反应后的混合物过滤,取滤液加入酚酞试液. | 酚酞试液变红色. | 证明猜想Ⅱ正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
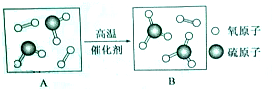
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
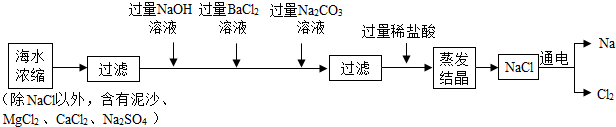
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 10.08g | B. | 10.18g | C. | 20.574g | D. | 20.674g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
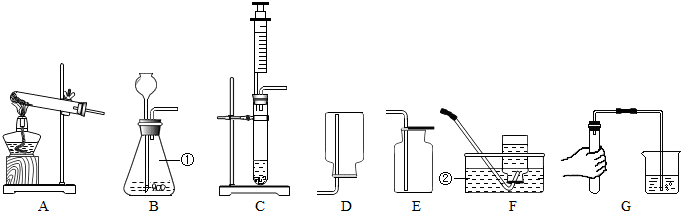
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量烧杯中的溶液于试管中,加入镁条 | 有气泡产生 | 猜想二正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com