某化学研究小组进行研究性学习,请你协助完成相关任务.
【研究课题1】探究水壶内部水垢的主要成分
【查阅资料】(1)天然水中含有Ca
2+、Mg
2+、HCO
3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).天然水和水垢所含的物质及其溶解性如下表:
| 物 质 |
Ca(HCO3)2 |
Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
MgCO3[来源:] |
| 溶解性 |
可溶 |
可溶 |
微溶 |
不溶 |
不溶 |
微溶 |
【提出猜想】水垢的主要成分一定含有Mg(OH)
2和
CaCO3
CaCO3
,可能含有Ca(OH)
2和MgCO
3.
【设计方案】
(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,静置.取上层清液滴入Na
2CO
3溶液,如果没有白色沉淀,说明水垢中无
Ca(OH)2
Ca(OH)2
(填化学式).
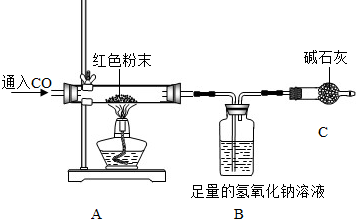
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分.

其主要实验步骤如下:
①按图组装仪器,将50g水垢试样放入锥形瓶中,逐滴加入足量稀盐酸.
②待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气,使装置内的气体缓缓通过后面的装置.
③称量D瓶内物质增加的质量;
④重复②和③的操作,直至D瓶内物质质量不变.
测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图曲线所示;
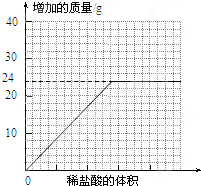
【思考与评价】
(1)当水中含较多可溶性钙、镁化合物的水叫硬水,生活中降低水的硬度的常用方法是:
煮沸
煮沸
.
(2)A瓶中的NaOH溶液作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳
.
(3)若50g水垢全部是碳酸钙,则最终应该产生二氧化碳的质量是
22
22
g.
(4)一般情况下,两种不同金属形成的碳酸盐与足量盐酸反应时,若两金属的化合价相同、两种盐的质量相同,则相对分子质量小者放出的气体多.分析曲线图可知:水垢中一定含有
MgCO3
MgCO3
(化学式),理由是
水垢中只有碳酸钙时只生二氧化碳质量是22克,实际生成CO2的质量是24g,大于
22g,所以水垢中一定含有碳酸镁
水垢中只有碳酸钙时只生二氧化碳质量是22克,实际生成CO2的质量是24g,大于
22g,所以水垢中一定含有碳酸镁
.
(5)以上实验
不能
不能
(填“能够”或“不能”)检测出水垢中含有Mg(OH)
2.
【研究课题2】为测定氯化钠样品的纯度,取30g氯化钠样品(杂质为氯化钙)溶于水配制成263g溶液,再加入53g溶质质量分数为20%的碳酸钠溶液,恰好完全反应.求:反应后所得溶液中溶质的质量分数.



 如图是A、B、C三种物质的溶解度曲线,根据溶解度曲线回答问题:
如图是A、B、C三种物质的溶解度曲线,根据溶解度曲线回答问题:
