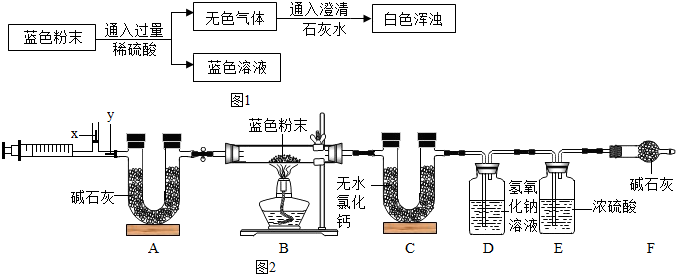
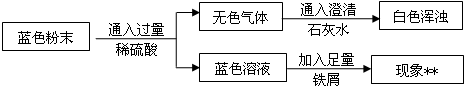
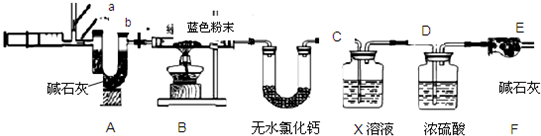
将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体.某研究性学习小组对蓝色固体的成分进行了如下探究.请完成下列各题:
(一)猜想与假设:(1)猜想一:固体为CuCO3,理由:_________ (用化学反应方程式表示).
(2)猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈_________(填“酸”或“碱”)性.猜想三:固体为Cu(OH)2和CuCO3的混合物.
(二)资料查阅:①Cu(OH)2和CuCO3晶体均不带结晶水;②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物.
(三)设计与实验:
Ⅰ.固体的获取:
(3)将反应后的固、液混合物经_________、洗涤、低温烘干得蓝色固体.
(4)判断固体已洗净的方法及现象_________.
Ⅱ.用下图所示装置,定性探究固体的成分.
(5)若用装置A、B组合进行实验,B中无现象,则猜想 _________ 正确;
(6)若用装置A、C组合进行实验,C中无现象,则猜想 _________ 正确;
(7)小组同学将装置按A、 _________ 、 _________ (填“B”、“C”)的顺序组合进行实验,验证出猜想三是正确的,实验中:
B中的现象为_________,
C中的现象为_________.
结论:固体为Cu(OH)2和CuCO3的混合物.
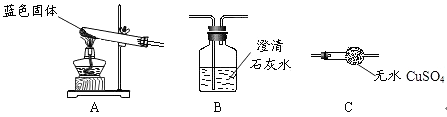
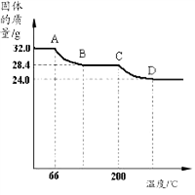
Ⅲ.固体成分定量测定:已知Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃.设固体的组成为aCu(OH)2.bCuCO3.小组同学用热分析仪对固体进行热分解,获得相关数据,绘成固体质量变化与分解温度的关系如图,请根据图示回答下列问题:
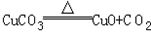
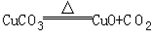
(8)写出A B、C D段发生反应的化学方程式:AB段:_________;CD段:_________;
(9)通过计算可得:a:b=_________.
(10)若将24.0g剩余固体继续加热到更高的温度,发现固体质量减少了2.4g后质量不再改变,写出此过程中可能发生反应的化学方程式:_________.


 ↑
↑
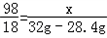
 ↑
↑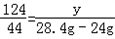
 =2:1
=2:1 =4.8g,大于2.4g,说明是氧化铜中的部分氧元素转化为氧气.
=4.8g,大于2.4g,说明是氧化铜中的部分氧元素转化为氧气.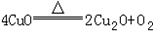 ↑
↑