
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有二氧化碳 | 含有CO和CO2 |
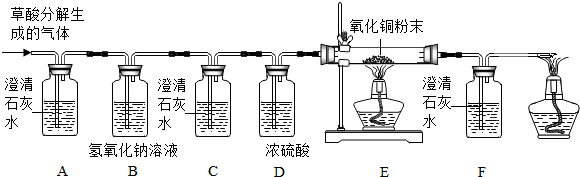
分析 【猜想】根据猜想1和3进行分析;
【设计实验】(1)A装置中的澄清石灰水变浑浊,能够证明有CO2气体;
(2)根据一氧化碳有还原性,能和氧化铜反应生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊进行分析;
【实验结论】根据猜想3成立可知,反应物、反应条件、生成物然后写出化学反应式即可;
【问题讨论】
(1)根据氢氧化钠溶液可以吸收二氧化碳气体,浓硫酸有吸水性进行分析;
(2)根据装置末端酒精灯可以处理尾气CO进行分析.
解答 解:【猜想】根据猜想1和3可知,猜想2是只有CO2;
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有二氧化碳 | 含有CO和CO2 |
点评 本题是检验一氧化碳和二氧化碳的存在,就要我们熟悉一氧化碳和二氧化碳的性质特点.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:初中化学 来源: 题型:选择题
| 物质 | 除杂质选用的试剂 | 操作方法 | |
| A | KCl固体(KClO3) | MnO2,H2O | 加热后加水溶解过滤、蒸发结晶 |
| B | H2(HCl) | Na2CO3溶液、浓H2SO4 | 吸收、干燥 |
| C | KNO3固体(KOH) | H2O、CuSO4溶液 | 溶解、过滤、蒸发结晶 |
| D | CaCl2溶液(HCl) | 过量的CaO | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 得出的结论 |
| 向步骤(1)的溶液中滴加过量的 稀盐酸溶液 | 开始没有明显变化,后来有气泡产生,最后溶液变成无色 | 猜想②成立,写出该反应的化学方程式: NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
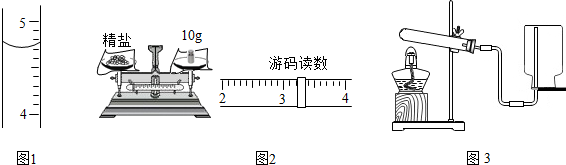
| A. | 0.20g | B. | 0.22g | C. | 0.18g | D. | 0.21g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com