
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5 g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.lg | I2.7g |
| 性质 | Na2CO3 | NaHCO3 | 性质比较 |
| 溶液的酸碱性 | 碱性 | 碱性 | 相铜条件下,Na2C03溶液的碱性更强 |
| 热稳定性 | 稳定 | 不稳定 | NaHCO3受热分解生成Na2C03、C02 和H20 |
| 与盐酸反应 | 反应 | 反应 | 均产生CO2,但NaHCO3与盐酸的反应更加剧烈 |
| 实验方案 | 实验现象及结论 1 |
| 方案一:20℃时,在100 g水中加入11 g该白色固体,充分溶解 | 若有白色固体剩余,样品为碳酸氢钠; 否则为碳酸钠. |
| 方案二:分别将两种待测固体溶于水制成5%的溶液,用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象 | pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液. |
| 方案三:分别取少量固体于試管中加热,将产生的气体通入澄清的石灰水中. | 若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠. |
| 方案四:如阁所示,分别将气球中的白色固体全部且同时倒入装有盐酸的试管中,观察现象. | 气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠 |
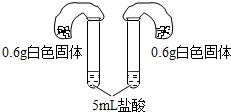 【实验反思】
【实验反思】分析 根据对碳酸钠与碳酸氢钠性质差别的认识,利用两物质性质的不同,设计实验鉴别两种物质.
解答 解:
可利用碳酸钠和碳酸氢钠在不同温度下的溶解度;碳酸钠与盐酸反应时会先生成碳酸氢钠而不会马上产生二氧化碳气体、碳酸氢钠受热能分解出气体二氧化碳或两物质所得溶液的酸碱性强弱有明显差异等性质,分别进行滴加盐酸、加热或测溶液pH等对比实验,进行鉴别;则:
【设计方案并实施】
| 实验方案 | 实验现象及结论 1 |
| 方案一:20℃时,在100g水中加入11g该白色固体,充分溶解 | 若有白色固体剩余,样品为碳酸氢钠; 否则为碳酸钠. |
| 方案二:分别将两种待测固体溶于水制成5%的溶液,用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象 | pH值大的为碳酸钠溶液,pH值小的为碳酸氢钠溶液. |
| 方案三:分别取少量固体于試管中加热,将产生的气体通入澄清的石灰水中. | 若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠. |
| 方案四:如阁所示,分别将气球中的白色固体全部且同时倒入装有盐酸的试管中,观察现象. | 气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠 |
| 实验方案 | 实验现象及结论 |
| 方案一:20℃时,在100g水中加入11g该白色固体,充分溶解. | |
| 方案二:用玻璃棒分别蘸取少量待测液于pH试纸上,静置,观察现象. | |
| 若石灰水变浑浊,样品为碳酸氢钠,否则为碳酸钠. | |
| 气球胀大速度快且大的,原固体为碳酸氢钠,否则为碳酸钠. |
点评 本题考查物质的鉴别,学生应注意利用物质性质的差异,多种方法并用来鉴别物质,将反应、现象、计算相结合来分析解答.


科目:初中化学 来源: 题型:选择题
| A. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 | |
| B. | 合理使用加碘盐有利于碘缺乏症病人健康 | |
| C. | 食用甲醛水溶液浸泡过的海产品对人身体无害 | |
| D. | 香烟的烟气中含有很多对人体有害的物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
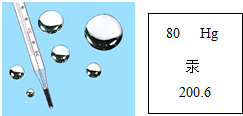 汞是银白色闪亮的重质液体,化学性质稳定,不溶于酸也不溶于碱.汞常温下即可蒸发,汞蒸发气和汞的化合物多有剧毒(慢性).汞使用的历史很悠久,用途很广泛,如图是汞在元素周期表中的相关信息,关于汞的说法正确的是( )
汞是银白色闪亮的重质液体,化学性质稳定,不溶于酸也不溶于碱.汞常温下即可蒸发,汞蒸发气和汞的化合物多有剧毒(慢性).汞使用的历史很悠久,用途很广泛,如图是汞在元素周期表中的相关信息,关于汞的说法正确的是( )| A. | 汞属于非金属元素 | |
| B. | 汞原子中质子与中子数之和为200.6 | |
| C. | 汞原子中电子数为80 | |
| D. | 汞不能与其他物质发生化学反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入稀盐酸,有无色气体产生的物质中一定有碳酸盐 | |
| B. | 经点燃,产生蓝色火焰的气体不一定是一氧化碳 | |
| C. | 能使紫色石蕊试液变红的一定是酸 | |
| D. | 用燃着的木条深入某气体中,火焰熄灭,则该气体一定是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
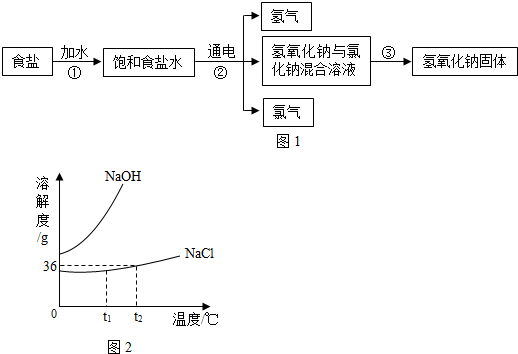
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
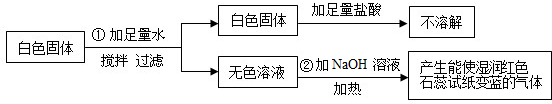
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com