
 小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.
小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 2.2 | m | 5.5 |
分析 由表中数据可知,第Ⅱ组反应中碳酸钠仍然过量,因此生成二氧化碳的质量是4.4g;
根据生成二氧化碳的质量可以计算碳酸钠的质量和生成的氯化钠的质量,根据沉淀的质量可以计算氯化钠的质量,进一步可以计算该混合液中碳酸钠的质量分数和该混合液中氯化钠的质量分数.
解答 解:(1)实验1中,第二组数据m为4.4g.
故填:4.4.
(2)解:设50g混合液中碳酸钠的质量为x,同时与盐酸反应生成氯化钠的质量为y,
分析数据可知,50g混合液中碳酸钠与盐酸完全反应生成5.5g二氧化碳,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 117 44
x y 5.5g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{5.5g}$,
x=13.25g,y=14.63g,
混合液中碳酸钠的质量分数为:$\frac{13.25g}{50g}$×100%=26.5%,
答:混合液中碳酸钠的质量分数为26.5%.
(3)设生成57.4g氯化银沉淀需要氯化钠的质量为z,
NaCl+AgNO3=AgCl↓+NaNO3,
58.5 143.5
z 57.4g
$\frac{58.5}{z}$=$\frac{143.5}{57.4g}$,
z=23.4g,
该混合液中氯化钠的质量为:23.4g-14.63g=8.77g,
该混合液中氯化钠的质量分数为:$\frac{8.77g}{50g}$×100%=17.5%,
答:该混合液中氯化钠的质量分数为17.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析表中数据的能力,计算时要注意规范性和准确性.


科目:初中化学 来源: 题型:解答题
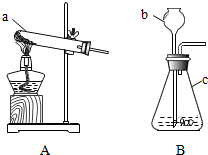 在实验室,同学们利用如图所示的装置来制取气体.
在实验室,同学们利用如图所示的装置来制取气体.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH+HNO3═NaNO3+H2O | B. | BaCl2+2KOH═Ba(OH)2↓+2KCl | ||
| C. | Fe+2KNO3═2K+Fe(NO3)2 | D. | Cu+2HCl═CuCl2+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
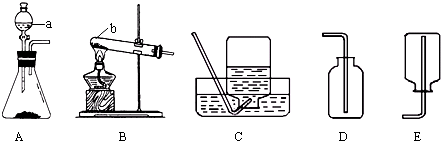
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
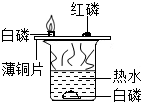 小王用如图所示的装置探究可燃物燃烧的条件.他发现热水中白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷不燃烧.请回答:
小王用如图所示的装置探究可燃物燃烧的条件.他发现热水中白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷不燃烧.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com