
分析 利用极值假设的方法,根据反应的化学方程式,计算合金完全反应产生氢气的量.
解答 解:当粉末为Fe-Al合金时,假设56g金属全部为铁
设生成氢气质量为x
Fe+H2SO4=FeSO4+H2↑
56 2
56g x
$\frac{56}{2}=\frac{56g}{x}$
解之得 x=2g
假设56g金属全部为铝,设生成氢气质量为y
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
56g y
$\frac{54}{6}=\frac{56g}{y}$
解之得 y≈6.2g
因此,当粉末为Fe-Al合金时,金属完全反应放出氢气质量6.2g>a>2g
当粉末为Cu-Fe合金时,假设56g金属全部为铁,则放出氢气质量为2g;
根据金属活动性,铜不能与稀硫酸反应;
因此,当粉末为Cu-Fe合金时,a<2g
故答案为:2;6.2;2.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力.


科目:初中化学 来源: 题型:实验探究题
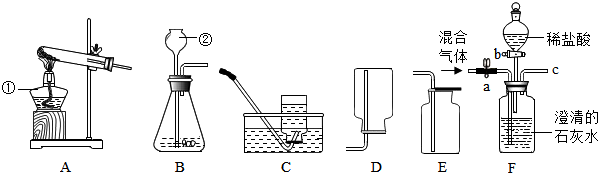
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化硫(SO2) | B. | 二氧化碳(CO2) | C. | 二氧化氮(NO2) | D. | 浮颗粒物(PM2.5) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
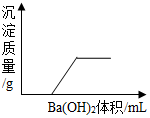 有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )| A. | 硝酸、硝酸铁 | B. | 硫酸、氯化铁 | C. | 盐酸、氯化铁 | D. | 盐酸、硫酸铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 我国食品安全法规定有些食品不允许添加防腐剂,因此有些食品包装中有一个单独包装的保鲜剂.某化学兴趣小组成员将家中一包(如图1)放置一段时间的食品保鲜剂带到学校,并邀兴趣小组的同学在化学实验室进行探究:
我国食品安全法规定有些食品不允许添加防腐剂,因此有些食品包装中有一个单独包装的保鲜剂.某化学兴趣小组成员将家中一包(如图1)放置一段时间的食品保鲜剂带到学校,并邀兴趣小组的同学在化学实验室进行探究:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ?取上述试管中的上层清液,滴加1─2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中含有Ca(OH)2 |
| ?往上述试管残留的白色固体中滴加稀盐酸 | 有气泡产生 | 白色粉末中含CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com