
(9分)化学课上第一小组的同学做了碳酸钠溶液和A溶液反应的实验,有沉淀产生,同学们对浑浊液过滤,得到澄清滤液。第二小组甲、乙、丙三位同学对该实验进行了一系列的探究。
探究一 A溶液中的溶质是什么?
【相关资料】Ⅰ.CaCl2 + Na2CO3 CaCO3↓+ 2NaCl Ⅱ.CaCl2溶液呈中性
(1)【提出假设】第二小组同学认为A溶液的溶质有两种可能:
①是_ __,②是 CaCl2 。
(2)【设计实验】第二小组同学设计了如下方案并进行实验:
|
实验操作 |
实验现象 |
实验结论 |
|
取少量A溶液于试管中,向其中滴加 溶液 |
__ |
假设①正确。 碳酸钠与其反应的化学方程式为__ 。 |
第一小组同学肯定了他们的实验结论。
探究二 过滤后澄清滤液中会有哪些溶质?
【提出假设】

(3)甲的合理猜想 ;丙的合理猜想 。
(4)【实验验证】乙同学针对自己的猜想进行了如下实验:
|
实验步骤 |
实验现象 |
实验结论 |
|
取样于试管中,滴入几滴稀盐酸 |
没有气体产生 |
猜想不成立 |
你认为乙同学的实验结论是否正确? ,其理由是 。
(5)【继续探究】请你设计实验方案确定滤液中溶质的组成。
|
实验操作 |
实验现象 |
实验结论 |
|
|
|
|
(1)(1分)Ca(OH)2
(2)(2分)(操作和现象1分,化学方程式1分)
|
实验操作 |
实验现象 |
实验结论 |
|
滴加 酚酞 溶液 |
__溶液变红 |
方程式为 Na2CO3+Ca(OH)2 CaCO3↓+2NaOH。 |
(3)(2分)甲:NaOH、Ca(OH)2 丙 :NaOH (答案可互换)
(4)(1分)不正确 溶液中有氢氧化钠,加入几滴盐酸,即使溶液中有碳酸钠,也可能不产生气体。
(5)(3分)
|
实验操作 |
实验现象 |
实验结论 |
|
分别取少量滤液于两支试管中,一支加入碳酸钠溶液,另一支加入氢氧化钙溶液 |
若加入碳酸钠溶液有沉淀产生 |
则滤液中的溶质是NaOH和Ca(OH)2 |
|
若加入氢氧化钙溶液有沉淀产生 |
滤液中的溶质是NaOH、Na2CO3
|
|
|
若两支试管中均无现象 |
则滤液中的溶质为NaOH |
【解析】
试题分析:
(1)【提出假设】第二小组同学认为A溶液的溶质有两种可能:
①是Ca(OH)2 ,②是CaCl2。因为氢氧化钙和氯化钙都能与碳酸钠反应生成沉淀。
(2)【设计实验】
|
实验操作 |
实验现象 |
实验结论 |
|
取少量A溶液于试管中,向其中滴加滴加 酚酞 溶液 |
溶液变红 |
假设①正确。 碳酸钠与其反应的化学方程式为方程式为 Na2CO3+Ca(OH)2 CaCO3↓+2NaOH。 |
【提出假设】
(3)甲的合理猜想是:NaOH、Ca(OH)2;丙的合理猜想是:NaOH。
(4)【实验验证】乙同学取样于试管中,滴入几滴稀盐酸,没有气体产生,并不能说明溶液中没有碳酸钠,因为溶液中有氢氧化钠,加入几滴盐酸,盐酸会先与氢氧化钠反应,故即使溶液中有碳酸钠,也可能不产生气体。
(5)【继续探究】设计实验方案确定滤液中溶质的组成。
|
实验操作 |
实验现象 |
实验结论 |
|
分别取少量滤液于两支试管中,一支加入碳酸钠溶液,另一支加入氢氧化钙溶液 |
若加入碳酸钠溶液有沉淀产生 |
则滤液中的溶质是NaOH和Ca(OH)2 |
|
若加入氢氧化钙溶液有沉淀产生 |
滤液中的溶质是NaOH、Na2CO3
|
|
|
若两支试管中均无现象 |
则滤液中的溶质为NaOH |
考点:物质推断;实验设计与探究;化学方程式;酸碱指示剂。
点评:鉴别、推断物质,要根据实验中,独特的实验现象来辨别,了解常见物质的性质就显得特别重要;书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:初中化学 来源: 题型:
 某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).查阅资料:草酸在浓硫酸存在时加热发生如下反应:H2C2O4| 浓硫酸 | △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
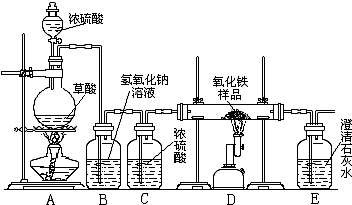
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
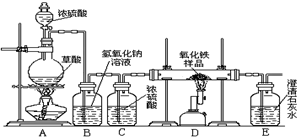 化学小组的同学在研究性学习课上展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应,且杂质中不含铁).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
化学小组的同学在研究性学习课上展示了一套如图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应,且杂质中不含铁).查阅资料:草酸在浓硫酸存在时加热发生如下反应:
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2007年第十七届“天原杯”全国初中学生化学素质和实验能力竞赛(山东赛区)初赛试卷(解析版) 题型:解答题
 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O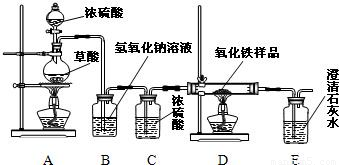
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com