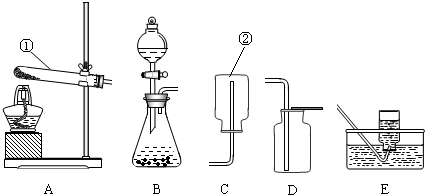
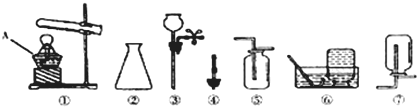
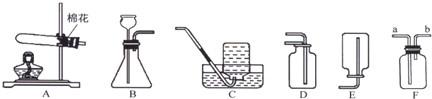
½ā“š£ŗ½ā£ŗ£Ø1£©¢ŁŹĒŹŌ¹Ü£»¢ŚŹĒ³¤¾±Ā©¶·£»
£Ø2£©øßĆĢĖį¼Ų¼ÓČČ·Ö½ā²śÉśĆĢĖį¼Ų”¢¶žŃõ»ÆĆĢŗĶŃõĘų£¬¹Ź·¢Éś×°ÖƵÄĢŲµćŹĒ¹ĢĢå¼ÓČČŠĶµÄB×°ÖĆ£»·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗ2KMnO
4K
2MnO
4+MnO
2+O
2”ü£»
£Ø3£©“óĄķŹÆŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆøĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗCaCO
3+2HClØTCaCl
2+H
2O+CO
2”ü£»·¢Éś×°ÖƵÄĢŲµćŹĒ¹ĢŅŗ³£ĪĀŠĶµÄC×°ÖĆ£¬ÓĆÅØĮņĖįøÉŌļ£¬¶žŃõ»ÆĢ¼µÄĆܶȱČæÕĘų“󣬹ŹÓĆĻņÉĻÅÅæÕĘų·ØŹÕ¼Æ£¬¹ŹŃ”ŌńCDE×é×°Ņ»Ģ×ÖĘČ”øÉŌļ¶žŃõ»ÆĢ¼µÄ×°ÖĆ£»
£Ø4£©½ā£ŗ¢ŁÉčĀČ»ÆøʵÄÖŹĮæĪŖX
CaCl
2+Na
2CO
3=CaCO
3”ż+2NaCl
111 100
X 5g
=
½āµĆX=5.55æĖ
¢ŚCaCl
2+Na
2CO
3=CaCO
3”ż+2NaCl
Na
2CO
3+2HClØT2NaCl+H
2O+CO
2ӟ
øł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬30gĢ¼ĖįÄĘČÜŅŗÖŠµÄÄĘŌŖĖŲÖŹĮæŗĶ×īÖÕ·“Ó¦ŗóµÄČÜŅŗÖŠµÄĀČ»ÆÄʵÄÄĘŌŖĖŲÖŹĮæŹĒĻąµČµÄ£¬ĻČĒó30gĢ¼ĖįÄĘČÜŅŗÖŠµÄÄĘŌŖĖŲµÄÖŹĮæĪŖ30”Į26.5%”Į
”Į100%=3.45g£¬
ŌņbµćŹ±ĀČ»ÆÄʵÄÖŹĮæĪŖ3.45g/£Ø
”Į100%£©=8.775g
“ĖŹ±ČÜŅŗµÄÖŹĮæĪŖ£ŗ50g+30g-5g-1.1g=73.9g
ĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ
”Į100%=11.9%
“š£ŗ50g·ĻŅŗÖŠŗ¬ĀČ»ÆøĘ5.55g£¬bµć±ķŹ¾µÄČÜŅŗÖŠĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ11.9%£®
¹Ź“š°øĪŖ£ŗ£Ø1£©ŹŌ¹Ü£»³¤¾±Ā©¶·£»
£Ø2£©B£» 2KMnO
4K
2MnO
4+MnO
2+O
2”ü£»
£Ø3£©CaCO
3+2HClØTCaCl
2+H
2O+CO
2”ü£»CDE£»
£Ø4£©½ā£ŗ¢ŁÉčĀČ»ÆøʵÄÖŹĮæĪŖX
CaCl
2+Na
2CO
3=CaCO
3”ż+2NaCl
111 100
X 5g
=
½āµĆX=5.55æĖ
¢ŚCaCl
2+Na
2CO
3=CaCO
3”ż+2NaCl
Na
2CO
3+2HClØT2NaCl+H
2O+CO
2ӟ
øł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬30gĢ¼ĖįÄĘČÜŅŗÖŠµÄÄĘŌŖĖŲÖŹĮæŗĶ×īÖÕ·“Ó¦ŗóµÄČÜŅŗÖŠµÄĀČ»ÆÄʵÄÄĘŌŖĖŲÖŹĮæŹĒĻąµČµÄ£¬ĻČĒó30gĢ¼ĖįÄĘČÜŅŗÖŠµÄÄĘŌŖĖŲµÄÖŹĮæĪŖ30”Į26.5%”Į
”Į100%=3.45g£¬
ŌņbµćŹ±ĀČ»ÆÄʵÄÖŹĮæĪŖ3.45g/£Ø
”Į100%£©=8.775g
“ĖŹ±ČÜŅŗµÄÖŹĮæĪŖ£ŗ50g+30g-5g-1.1g=73.9g
ĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ
”Į100%=11.9%
“š£ŗ50g·ĻŅŗÖŠŗ¬ĀČ»ÆøĘ5.55g£¬bµć±ķŹ¾µÄČÜŅŗÖŠĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ11.9%£®




 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø