
【题目】下列表中的叙述,对应的化学方程式和所属反应基本类型都正确的是( )
选项 | 叙述 | 化学反应方程式 | 反应类型 |
A | 电解水 |
| 分解反应 |
B | 探究一氧化碳的还原性 |
| 置换反应 |
C | 酸雨形成的原因 |
| 化合反应 |
D | 硫酸铜溶液中滴加氢氧化钠溶液 |
| 复分解反应 |
A.AB.BC.CD.D
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:初中化学 来源: 题型:
【题目】溶液在生产、生活中起着十分重要的作用。某学习小组的同学对溶液的性质进行探究。
(引发思考)生理盐水是医疗上常用的一种溶液,100mL生理盐水(其密度可近似看做1g/cm3)中含有0.9g医用氯化钠,该溶液中溶质的质量分数为______。一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是______。
(提出问题)溶液的某些性质是否可以通过定量实验进行验证?
(查阅资料)电导率传感器用于测量溶液的导电性强弱;一定条件下,电导率的大小能反映离子浓度的大小。
(实验探究1)氯化钠溶于水形成溶液的过程中氯离子浓度、电导率的测定。
第一步:读取室温为26℃,取100mL蒸馏水,加入烧杯中,放入磁力搅拌器磁珠;
第二步:校准传感器,组装仪器,设定搅拌档位;
第三步:用氯离子传感器和电导率传感器同时采集数据,迅速将一定质量的氯化钠加入烧杯中。实验数据如图所示。

分析图1实验数据:
(1)a-b段曲线呈这种形态的原因是______。
(2)请说明实验过程中液体的电导率变化的原因_________。
(交流反思1)如何通过实验验证氯化钠溶液是均一的?请简要说明。___________。
(实验探究2)用氯离子传感器和电导率传感器同时采集数据,向一定体积、一定浓度的氯化钠溶液中慢慢加入等体积、一定浓度的硝酸银溶液恰好完全反应。部分实验数据如图所示。
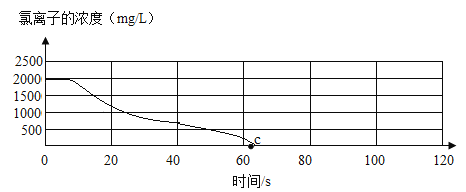
(交流反思2)推测c点时溶液的电导率是否为零,并说明理由。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )

A. a的溶解度大于b的溶解度
B. P点表示t1℃时a、c两物质溶解度相等
C. 将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液
D. 将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质最分数由大到小的顺序为:b>a=c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粗盐中含有泥沙等不溶性杂质,还含有氯化钙、氯化镁、硫酸钠等可溶性杂质。提纯粗盐并制取纯碱的工艺流程如下:
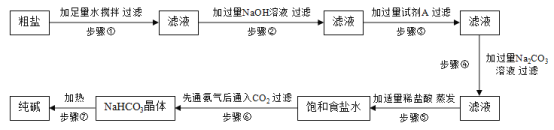
已知:①20℃时,将CO2通入含有NH3的饱和NaCl溶液中生成NaHCO3晶体和NH4Cl溶液
②20℃时,几种物质在水中的溶解度/g
NaCl | NH4Cl | NaHCO3 |
36.0 | 37.2 | 9.6 |
请根据上述题中有关信息,回答下列问题:
(1)步骤③中加入试剂A的化学式是_____。
(2)步骤④中加入过量Na2CO3溶液的目的是_____。
(3)在步骤⑥反应中,有NaHCO3晶体析出,而没有NH4Cl和NaCl析出的原因是_____。
(4)步骤⑦中NaHCO3,转化为纯碱的化学反应方程式是![]() ,该化学反应属于反应_____〔填基本反应类型)。
,该化学反应属于反应_____〔填基本反应类型)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在2020年春节伊始,我国爆发了新型冠状病毒肺炎,给人民的生命带来严重的威胁,给国家人民的财产带来严重的损失,全国人民众志成城抗击新型冠状病毒肺炎。在众多的措施中有一条就是要勤消毒。84消毒液有效成分为次氯酸钠和二氧化氯(ClO2),是常用消毒剂。
(1)将氯气通入氢氧化钠溶液中可以得到次氯酸钠,根据反应原理推断次氯酸钠的化学式。其反应原理:Cl2 + 2NaOH= NaCl +H2O + ______,次氯酸钠中氯元素的化合价____;
(2)次氯酸钠属于_____________(填序号)。
A 酸 B 碱 C 氧化物 D 盐
(3)次氯酸钠固体在光照的情况下分解为一种常见的化学物质和空气中体积分数为21%的气体,写出其化学反应方程式:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了除去NaCI溶液中含有少最的MgC12、CaC12和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如图所示的实验。
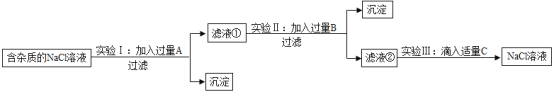
回答下列问题:
(1)实验I中加入试剂A除去的杂质是_____;
(2)实验II中加入的试剂B是_____溶液;
(3)滤液②中除Na+和Cl-外,还含有的离子是_____(填离子符号);
(4)实验III中发生的中和反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有化学实验考试后留下混有少量食盐的小苏打( NaHCO3)样品。现称取样品10克,加入某溶质质量分数的稀盐酸90克,至充分反应不再有气泡产生为止,称得剩余溶液质量为96.04克。求:
(1)生成气体的质量;
(2)样品中 NaHCO3的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳和碳的化合物是化学物质世界中庞大的家族。
(1)活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,原因是活性炭具有______性。生产N95口罩的主要原料是聚丙烯[(C3H6)n],聚丙烯_____(填“属于”或“不属于”)有机合成材料。
(2)随着化石燃料的大量使用带来的是环境的污染和资源的枯竭等问题。国家已经全面推广使用车用乙醇汽油。乙醇燃烧的化学方程式是_______。
(3)我国大力发展低碳经济,导低碳生活。所谓“低碳”,就是较低的______(填化学式)排放。
(4)下图是自然界中的碳、氧循环示意图。下列说法中一定正确的是_______(填序号)。

A 大气中的O2越多越好,CO2越少越好
B 化石燃料燃烧时化学能可以转化为热能和光能
C 绿色植物的生长过程,既涉及碳循环,又涉及氧循环
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以FeSO4·7H2O为原料制备铁红(Fe2O3)的一种方法如下:

已知“沉淀”时的主要反应为:![]()
(1)FeO(OH)中铁元素的化合价为_______。FeO(OH)可表示为mFe2O3·nFe(OH)3,![]() =_____________。
=_____________。
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有__________(填字母)。
A 能与酸反应
B 能与碱反应
C 不与FeO(OH)反应
②“沉淀”时反应温度不宜过高,其原因是_______。
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为__________(填离子符号)。
(4)“煅烧”时反应的化学方程式为________。
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是___________。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是_______。
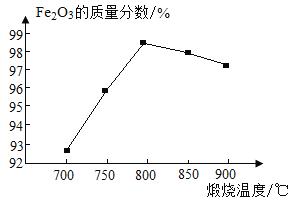
(6)用该方法制备Fe2O3,计算理论上13.9 t FeSO4·7H2O(相对分子质量为278)可制得Fe2O3的质量(写出计算过程)。_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com