
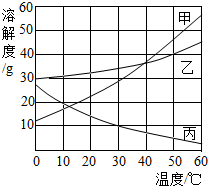
 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题: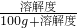 ×100%,所以饱和溶液的质量分数大小取决于溶解度的大小,因为在10℃时溶解度大小为:乙>丙>甲,所以饱和溶液质量分数也是乙>丙>甲,升温到50℃,甲和乙溶解度都变大,变为不饱和溶液,溶质质量分数不变,所以还是乙>甲,丙物质升温后溶解度减小,会析出晶体,丙物质的溶解度要按照50℃时丙的溶解度计算,因为10℃时甲的溶解度大于50℃时丙的溶解度,所以升温后甲的溶质质量分数大于丙物质的溶质质量分数,所以50℃时
×100%,所以饱和溶液的质量分数大小取决于溶解度的大小,因为在10℃时溶解度大小为:乙>丙>甲,所以饱和溶液质量分数也是乙>丙>甲,升温到50℃,甲和乙溶解度都变大,变为不饱和溶液,溶质质量分数不变,所以还是乙>甲,丙物质升温后溶解度减小,会析出晶体,丙物质的溶解度要按照50℃时丙的溶解度计算,因为10℃时甲的溶解度大于50℃时丙的溶解度,所以升温后甲的溶质质量分数大于丙物质的溶质质量分数,所以50℃时

 口算题天天练系列答案
口算题天天练系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?南漳县模拟)运用溶解度表与溶解度曲线回答下列问题:
(2013?南漳县模拟)运用溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
 运用溶解度表与溶解度曲线回答下列问题:
运用溶解度表与溶解度曲线回答下列问题:| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.3 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com