


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
| A、N2中的O2(灼热铜丝) |
| B、CaO中的CaCO3(高温煅烧) |
| C、CO2中的CO(点燃) |
| D、Na2SO4溶液中的Na2CO3(H2SO4) |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入 | 猜想三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
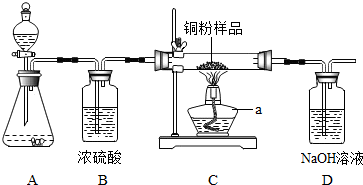
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL 5%H2O2溶液的试管. | 带火星木条不复燃 | H202溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H202溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管.观察现象.待反应结束后将试管里的剩余物进行 | 称得固体质量为1g. | 猜想Ⅰ成立.反应前后氧化铜的质量相等. |
| 实验三:向盛有5mL5%H202溶液的试管中加入1g | 没有气泡产生,带火星 木条不复燃. | 猜想Ⅱ |
查看答案和解析>>
科目:初中化学 来源: 题型:
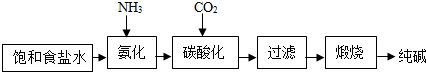
| ||
| 实验步骤 | 实验现象 | 实验结论 |
①如图装置,把少量样品放入a试管中加热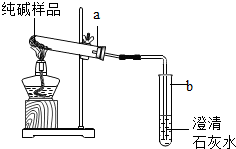 | ②b试管澄清石灰水 没变浑浊 | ③纯碱样品中 |
| ④取样品少量,溶解,加足量稀硝酸,再滴加硝酸银溶液 | ⑤ | ⑥纯碱样品中有NaCl |
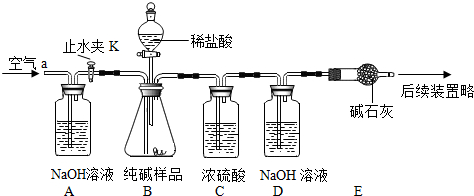
查看答案和解析>>
科目:初中化学 来源: 题型:
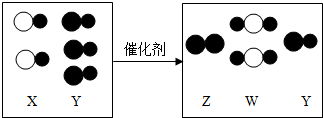
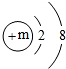 ,其微粒符号可表示为A2-,则m的值为
,其微粒符号可表示为A2-,则m的值为查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、实验结束后,剩余的药品要放回原瓶,避免浪费 |
| B、实验室里可用品尝的方法区分食盐和蔗糖 |
| C、过滤时漏斗内液体液面要低于滤纸边缘 |
| D、测定溶液pH时,将pH试纸直接浸入待测液中,显色后,取出与标准比色卡比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com