
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| 氧气体积/cm3 | 0 | 48 | 70 | 82 | 88 | 88 |
| 平均反应速率/cm3 s-1 | 0.0 | 2.4 | 1.1 | ① 0.6 | 0.3 | 0.0 |
分析 (1)根据上述表格中的数据可以进行相关方面的计算;
(2)催化剂能够改变化学反应的速率,而与最终产生氧气质量多少无关;
(3)氧气质量=氧气密度×氧气体积.
解答 解:(1)上述表格中①代表的数据是:(82-70)÷20=0.6,
故填:0.6.
(2)如果重做以上实验,并用1.0gMnO2做催化剂,最终产生的氧气总量不变,理由是:二氧化锰能够改变过氧化氢的分解速率,而与最终产生氧气的总质量无关,两次过氧化氢质量相等,因此产生氧气质量相等.
故填:不变;二氧化锰能够改变过氧化氢的分解速率,而与最终产生氧气的总质量无关,两次过氧化氢质量相等,因此产生氧气质量相等.
(3)该实验条件下,最终产生的氧气质量是:1.33g/L×0.088L=0.12g,
故填:0.12.
点评 催化剂能够改变化学反应的速率,而本身质量和化学性质在反应前后都不变,要注意理解.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 | 试管1 | 试管2 |
| 操作 | 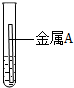 | 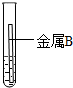 |
| 现象 | 金属表面产生气泡较慢 | 金属表面产生气泡较快 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
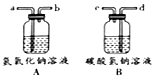 反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:
反应物的温度、浓度、固体反应物的颗粒大小等因素会影响化学反应速率.为研究实验室制取二氧化碳的适宜条件,进行如下四组实验:| 甲 | 乙 | 丙 | 丁 | |
| 大理石/(等量) | 块状 | 块状 | 粉末状 | 粉末状 |
| 盐酸/(质量分数) | 5% | 10% | 5% | 10% |
| 收集50mL二氧化碳所需时间/(秒) | 118 | 60 | 70 | 50 |
| 时段 | 第10秒 | 第20秒 | 第30秒 | 第40秒 | 第50秒 | 第60秒 |
| CO2体积 | 13 | 11 | 9 | 8 | 5 | 4 |
| 甲 | 乙 | |
| 大理石/(等量) | 块状 | 块状 |
| 盐酸/(质量分数) | 10% | 10% |
| 盐酸质量/(g) | 100 | 100 |
| 盐酸温度/℃ | 20 | 30 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质总质量/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
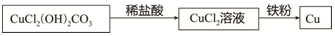
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度(克) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | 138 | 169 |
| A. | 升温 | B. | 降温 | C. | 加糖 | D. | 搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com