16g氧化铁(Fe2O3)中所含氧元素的质量与多少g硫酸(H2SO4)中所含氧元素质量相等?
【答案】
分析:只有熟悉只有熟悉化学式的意义、有关化学式的计算方法,才能得出本题的正确答案.
解答:解:16g氧化铁中氧元素的质量为16g×(
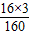
×100%)=4.8g
由于氧化铁与硫酸中所含氧元素的质量相等,因此硫酸中所含氧元素的质量也是4.8g.
因此含4.8g氧元素的硫酸的质量为4.8g÷(
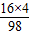
×100%)=7.35g
答:16g氧化铁(Fe
2O
3)中所含氧元素的质量与7.35g硫酸(H
2SO
4)中所含氧元素质量相等.
点评:本题主要考查有关化学式的计算中元素质量分数的计算、元素质量的计算、化合物质量的计算,难度稍大.
