
(2007?兰州)下列除去杂质的方法中,正确的是( )
|


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
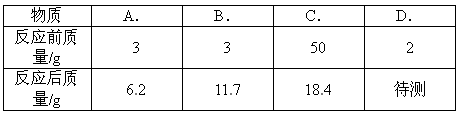
(2007?兰州)在一密闭容器中有A、B、C、D四种物质,一定条件下使之反应,一段时间后,测得反应前后各物质的质量如表所示.则该密闭容器中发生的化学反应类型为( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 配料 | 氯化钠、碘酸钾(KIO3) |
| 含碘量 | (20mg~30mg)/kg食盐 |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避光、避热、密封、防潮 |
查看答案和解析>>
科目:初中化学 来源: 题型:038
(2007
,兰州,33)新华网3月22日报道:“由于气候变暖的影响,南极冰山融化的速度加快,温度的升高已经开始深深影响到南极的冰山形状.”造成全球气候变暖的主要原因可能是大量排放二氧化碳等温室气体造成的,控制日趋严重的温室效应已势在必行.(1)
科学家采取“组合转化”技术,将 和
和 以一定比例混合,在一定条件下反应,生成一种重要的化工原料——乙烯
以一定比例混合,在一定条件下反应,生成一种重要的化工原料——乙烯 和水.请写出该反应的化学方程式:___________________________________________.
和水.请写出该反应的化学方程式:___________________________________________.
(2)
为了减缓大气中 含量的增加,以下建议可行的是(填序号)________.
含量的增加,以下建议可行的是(填序号)________.
①开发太阳能、水能,风能、地热等新能源;②禁止使用煤、石油、天然气等矿物燃料;③大量植树造林,禁止乱砍滥伐.
查看答案和解析>>
科目:初中化学 来源: 题型:013
(2007
,兰州)在一密闭容器中有A、B、C、D四种物质,一定条件下使之反应,一段时间后,测得反应前后各物质的质量如下表所示.则该密闭容器中发生的化学反应类型为[
]
|
A .化合反应 |
B .置换反应 |
|
C .分解反应 |
C .复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com