
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
| 装置B | 装置C | 装置D | |
| 实验前物质的质量/g | 180.0 | 200.0 | 122.2 |
| 实验后物质的质量/g | 176.9 | 201.5 | 124.8 |
分析 【探究一】根据20℃时碳酸钠和碳酸氢钠的溶解度进行分析;
【探究二】
【方案一】
(1)根据碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳进行分析;
(2)根据加热至恒重可以使碳酸氢钠完全分解进行分析;
[方案二]:
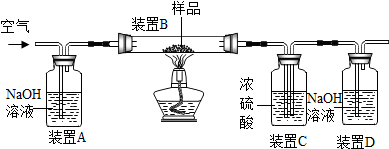
①根据浓硫酸有吸水性,洗气时应该是长进短出进行分析;
②根据二氧化碳和氢氧化钠反应生成碳酸钠和水进行分析
【讨论分析】根据溶液中会挥发出水蒸气,导致测定结果偏大来分析,空气中含有二氧化碳来分析;根据实验数据来分析解答,固体减少的质量就是碳酸氢钠分解生成水和二氧化碳的总质量;
【数据处理】根据题中的数据,结合化学方程式进行计算;
【拓展应用】根据碳酸氢钠受热会分解生成碳酸钠、水和二氧化碳进行分析.
解答 解:
【探究一】20℃时碳酸钠和碳酸氢钠的溶解度分别为21.5g和9.6g,那么在该温度下,10g水中最多溶解2.15g碳酸钠达到饱和,最多溶解0.96g碳酸氢钠达到饱和,因此可分别加入2g固体,充分搅拌后,若完全溶解则为碳酸钠,若不能完全溶解则为碳酸氢钠,故选:A;
【探究二】
[方案一]
(1)碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(2)加热至恒重可以使碳酸氢钠完全分解;
[方案二]:
①浓硫酸有吸水性,洗气时应该是长进短出,所以装置C的作用是吸收水蒸气,装置C中一个明显的错误是:右侧导管伸入液面以下;
②空气经过装置A时,其中的二氧化碳与氢氧化钠反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O,若没有此装置,则装置D增重偏大,认为生成的二氧化碳质量偏大,造成测定结果偏大;
【讨论分析】小张认为不能用C装置的质量变化来计算,其理由是:装置A中逸出的水蒸气会进入装置C中,改进方法是:在装置A、B之间增加一个浓硫酸的干燥装置,小王又认为用装置D的质量差会偏大而影响计算,应增加一个操作:连接D装置前,缓缓鼓入空气,目的是:排尽装置内的二氧化碳气体;
【数据处理】解:设其中含碳酸氢钠的质量为x
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
168 (18+44=62)
x 180.0g-176.9g=3.1g
$\frac{168}{x}=\frac{62}{3.1g}$
x=8.4g
NaHCO3和Na2CO3混合物中NaHCO3的质量分数为:$\frac{8.4g}{10g}$×100%x=8.4g
【拓展应用】碳酸氢钠受热会分解生成碳酸钠、水和二氧化碳,所以固体Na2CO3中混有少量NaHCO3,可通过加热方法除去.
故答案为:
【探究一】A
【探究二】
[方案一](1)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑(2)保证NaHCO3 全部分解;
[方案二]
①除去水蒸气;右侧导管伸入液面以下;
②2NaOH+CO2=Na2CO3+H2O;偏大;
【讨论分析】装置A中逸出的水蒸气会进入装置C中;在装置A、B之间增加一个浓硫酸的干燥装置;连接D装置前,缓缓鼓入空气;排尽装置内的二氧化碳气体;
【数据处理】84%.
【拓展应用】加热
点评 本题考查碳酸氢钠含量的测定实验,为高频考点,把握实验装置的作用及实验目的为解答的关键,侧重分析、计算及实验能力的综合考查,题目难度中等.


科目:初中化学 来源: 题型:选择题
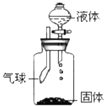 用如图的装置进行实验,使固体与液体接触,能够观察到气球先膨胀,过一段时间又恢复到原状,符合条件的一组物质是( )
用如图的装置进行实验,使固体与液体接触,能够观察到气球先膨胀,过一段时间又恢复到原状,符合条件的一组物质是( )| A. | 硝酸铵和水 | B. | 生石灰和水 | ||
| C. | 碳酸钠和稀盐酸 | D. | 二氧化锰和过氧化氢溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该气体一定含有H2、CO、CH4 | B. | 该气体可能只含H2、CH4 | ||
| C. | 该气体可能只含CO、CH4 | D. | 该气体可能只含CH4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列分析错误的是( )| A. | 50℃时,A物质的溶解度最大 | |
| B. | 50℃时,把90gA物质放入100g水中能得到190g溶液 | |
| C. | 20℃时,B物质饱和溶液的溶质质量分数最大 | |
| D. | 升温可使C物质的不饱和溶液变成饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
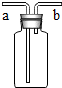 (1)若用如图所示正放的装置收集氧气,则氧气应从a(填“a”或“b”下同)端通入;若用装满水的正放的该装置收集氧气,则氧气应从b端通入;
(1)若用如图所示正放的装置收集氧气,则氧气应从a(填“a”或“b”下同)端通入;若用装满水的正放的该装置收集氧气,则氧气应从b端通入;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生活中通过煮沸可以降低水的硬度 | |
| B. | 经常饮用蒸馏水对身体有益无害 | |
| C. | 水中Ca2+、Mg2+增多导致水体富营养化 | |
| D. | 水是由氢气、氧气组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C和CO都可以将CuO中的Cu置换出来 | |
| B. | 在一定条件下CO2与CO可以相互转化 | |
| C. | 金刚石、石墨和C60都属于碳单质、但物理性质差异很大 | |
| D. | 温室效应既可以体现CO2的功,又可以体现CO2的过 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com