

| 称量项目 | 称量时间 | 质量(g) |
| 试样 | ---- | 10.00 |
| 装置+稀硫酸质量 | ---- | 241.20 |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
| 106 |
| 10.00g×x |
| 44 |
| 2.20g |


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
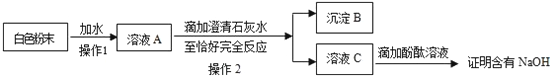
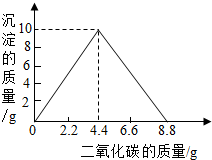 某实验小组在一定量的石灰水中通入CO2,产生沉淀的质量与通入CO2质量的关系如图所示.已知反应CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2易溶于水.
某实验小组在一定量的石灰水中通入CO2,产生沉淀的质量与通入CO2质量的关系如图所示.已知反应CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2易溶于水.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 金属 | Mn | Zn | Cu |
| 与盐酸反应现象 | 快速产生气泡 | 产生气泡 | 无气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 钙元素对人类生活具有重要意义.
钙元素对人类生活具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com