

分析 提【】出猜想】:进行猜想要考虑到反应前后元素种类不变;
【方案设计】
(1)根据质量守恒定律考虑;
(2)根据题中信息结合化学方程式的写法考虑;
(3)实验探究:点燃可燃性气体和空气的混合物容易发生爆炸;
【结论】:根据实验现象分析实验结论;
【思维拓展】:因为加入金属铁有氢气生成,所以溶液中可能含有酸.
解答 解:铁粉投入硫酸铜溶液中,反应前含有S、O、H、Cu元素,依据质量守恒定律可以得出猜想;
故答案为:质量守恒定律;
【方案设计】
(1)氧气具有助燃性,可以通过检验气体的助燃效果进行判断;
故答案为:用带火星的木条检验,看木条是否复燃;
(2)二氧化硫和氢氧化钙反应会生成亚硫酸钙和水;
故答案为:SO2+Ca(OH)2=CaSO3↓+H2O;
(3)实验探究:可燃性的气体和空气混合加热时可能会发生爆炸,因此先将收集到的气体从a通入一段时间后,再点燃C处酒精灯的目的是排出装置内的空气,以防加热时爆炸;
故答案为:排出装置内的空气,以防加热时爆炸;
【结论】:A装置中溶液不变浑浊,说明没有二氧化硫,H2可以使CuO还原成红色的Cu,故产生的气体为氢气;
故答案为:氢气;
思维拓展:因为有氢气生成,铁应该与酸反应产生氢气,故答案为:酸.
答案:
【提出猜想】质量守恒定律;
【方案设计】
(1)用带火星的木条检验,看木条是否复燃;
(2)SO2+Ca(OH)2=CaSO3↓+H2O;
(3)排出装置内的空气,以防加热时爆炸;
【结论】氢气;
【思维拓展】酸.
点评 本题主要考查化学实验的方案设计与评价,在解此类题时,首先分析题中考查的问题,然后结合所给的知识和学过的知识进行分析解答.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:初中化学 来源: 题型:选择题
 ”代表碳原子“
”代表碳原子“ ”代表氧原子).下列叙述中不正确的是( )
”代表氧原子).下列叙述中不正确的是( )| 物质 | M | N | X | Y |
| 微观示意图 | 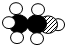 |  | 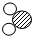 |  |
| A. | M、X、Y均为化合物 | |
| B. | M中碳、氢、氧三种元索质量比为12:3:8 | |
| C. | 在该反应中,生成X和Y的质量比为9:22 | |
| D. | 在该反应中,消耗掉M和N两种物质的分子个数比为1:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 主食 | 米饭 |
| 副食 | 红烧牛肉、清蒸鱼、猪蹄 |
| 饮料 | 酸牛奶 |
| A. | 炒鸡蛋 | B. | 烧排骨 | C. | 炖豆腐 | D. | 炒青菜 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
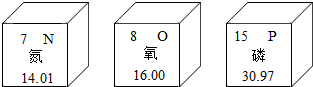
| A. | 氧元素的核电荷数为8 | |
| B. | 空气中含量最多的物质是氧元素的单质 | |
| C. | 磷原子的相对原子质量为30.97 | |
| D. | 氮元素和氧元素在同一周期 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
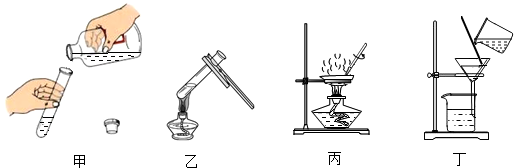
| A. | 如图甲取稀硫酸 | B. | 用装置乙加热反应物 | ||
| C. | 用装置丙蒸发浓缩 | D. | 用装置丁分离硫酸铜晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:
小明暑假期间到农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味.他很好奇,返校后和同学们进行探究,请你一同参与:| 实验步骤 | 实验现象 | 反应的化学方程式 |
| 取装置B中溶液少许,滴加稀盐酸(或滴加氯化钙溶液或氢氧化钡溶液) | 产生气泡(或产生白色沉淀) | Na2CO3+2HCl═2NaCl+CO2↑+H2O [或Na2CO3+CaCl2═CaCO3↓+2NaCl Na2CO3+Ba(OH)2═BaCO3↓+2NaOH] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com