
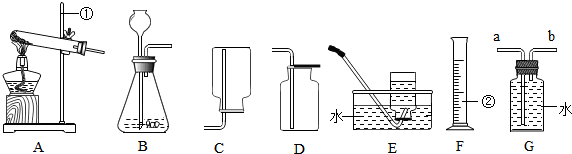
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据测定收集氧气的体积需要用排水法和用量筒量取排出水的体积进行分析;
(3)根据硫化氢和氢氧化钠反应生成硫化钠和水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是铁架台,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以发生装置可选A,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=H2O+CO2↑+CaCl2;
(2)测定收集氧气的体积需要用排水法和用量筒量取排出水的体积,所以可以选用的装置是:FG;
(3)硫化氢和氢氧化钠反应生成硫化钠和水,化学方程式为:2NaOH+H2S=Na2S+2H2O.
故答案为:(1)铁架台,A,CaCO3+2HCl=H2O+CO2↑+CaCl2;
(2)FG;
(3)2NaOH+H2S=Na2S+2H2O.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
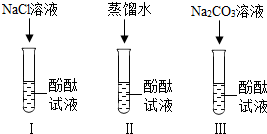 小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题:
小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请你、小宁和小明一起探究并完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1-2mL | B. | 试管容积的$\frac{1}{2}$ | C. | 试管容积的$\frac{1}{3}$ | D. | 4mL |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  在盐酸中加入氯化铁溶液,然后向其中逐滴加入NaOH溶液 | |
| B. |  在烧碱溶液中加入硝酸钡溶液,然后向其中逐滴加入稀硫酸 | |
| C. |  在烧碱溶液中加入碳酸钠溶液,然后向其中逐滴加入稀盐酸 | |
| D. |  在烧碱溶液中加入氧化铜固体,然后向其中逐滴加入稀硫酸并微热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 桐桐采集了一块石灰石样品,该样品杂质只含二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).
桐桐采集了一块石灰石样品,该样品杂质只含二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com